
| A. | 原子序数为34 | B. | 氢化物比HBr稳定 | ||
| C. | 非金属性比硫强 | D. | 最高价氧化物的水化物显碱性 |
分析 A、同主族相邻的3、4两周期元素原子序数差18;
B、同周期从左到右元素的氢化物稳定性逐渐增强;
C、同主族从上到下元素的非金属性逐渐减弱;
D、同主族从上到下元素的最高价氧化物的水化物碱性逐渐增强,酸性减弱.
解答 解:A、同主族相邻的3、4两周期元素原子序数差18,硫是16号,所以硒是34号,即原子序数为34,故A正确;
B、溴和硒同周期,同周期从左到右元素的非金属性逐渐增强,所以硒的氢化物不如HBr稳定,故B错误;
C、硒(Se)和硫同主族,同主族从上到下元素的非金属性逐渐减弱,所以硒(Se)的非金属性比硫弱,故C错误;
D、硒(Se)和硫同主族,硫的最高价氧化物的水化物硫酸是强酸性的,硒的最高价氧化物的水化物也显酸性,故D错误.
故选A.
点评 本题考查学生元素性质的递变规律,侧重于同主族元素性质的相似性和递变性,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | NO3- | B. | CO32-、NO3- | C. | SO32-、NO3- | D. | CO32-、NO3-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
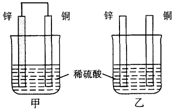
| A. | 两烧杯中铜片表面均无气泡产生 | B. | 甲中铜片是正极,乙中铜片是负极 | ||
| C. | 两烧杯中硫酸溶液的浓度均下降 | D. | 产生气泡的速度甲比乙慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2在正极发生氧化反应 | |
| B. | 供电时的总反应是 2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$ 2H2O | |
| C. | 氢氧燃料电池中反应放出的热量转变为电能 | |
| D. | 产物是无污染的水,属于环境友好电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,F元素原子的电子排布式1s22s22p63s23p5,E元素的原子结构示意图是
,F元素原子的电子排布式1s22s22p63s23p5,E元素的原子结构示意图是
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 在一体积为10L的容器中,通入一定量的CO和H2O,850℃时发生反应:CO(g)+H2O(g)?CO2(g)+H2(g).CO和H2O浓度变化如图所示:
在一体积为10L的容器中,通入一定量的CO和H2O,850℃时发生反应:CO(g)+H2O(g)?CO2(g)+H2(g).CO和H2O浓度变化如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 氮是地球上极为丰富的元素.
氮是地球上极为丰富的元素.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤ | B. | ②⑤⑥ | C. | ② | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com