
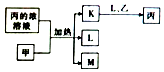
 短周期主族元素W、X、Y、Z的原子序数依次增加,K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体.K是无色气体,是主要的大气污染物之一,0.05mol/L丙溶液的pH为l,上述物质的转化关系如图所示.下列说法正确的是( )
短周期主族元素W、X、Y、Z的原子序数依次增加,K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体.K是无色气体,是主要的大气污染物之一,0.05mol/L丙溶液的pH为l,上述物质的转化关系如图所示.下列说法正确的是( )| A. | 原子半径:W<X<Y | B. | 元素的非全属性:Z>Y>X | ||
| C. | 化合物XYZ中只含共价键 | D. | K、L、M中沸点最高的是M |
分析 0.05mol/L丙溶液的pH为l,可知丙为二元强酸,应为H2SO4,K是无色气体,是主要的大气污染物之一,且可生成H2SO4,则应为SO2,可知乙为O2,L为H2O,乙是常见的气体,且与浓硫酸和甲反应生成,可知甲为C,M为CO2,则W为H元素,X为C元素,Y为O元素,Z为S元素,以此解答该题.
解答 解:W为H元素,X为C元素,Y为O元素,Z为S元素,
A.同周期元素原子半径从左到右逐渐减小,C>O,故A错误;
B.同主族元素从上到下非金属性减弱,O>S,故B错误;
C.化合物COS都由非金属性构成,只含共价键,故C正确;
D.K、M常温下为气体,L为水,常温下为液体,沸点最高,故D错误.
故选C.
点评 本题考查元素化合物推断,为高频考点,侧重考查学生的分析能力,注意溶液pH为推断突破口,需要学生熟练掌握元素化合物知识,注意抓住短周期元素形成二元化合物,难度不大.


科目:高中化学 来源: 题型:解答题
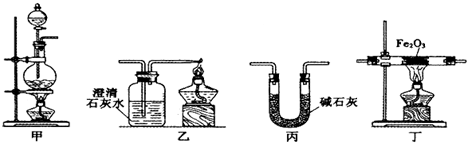
| 加热方式 | 通CO加热 时间/min | 澄清石灰水变 浑浊时间/min | 产物颜色 | 产物能否全部 被磁铁吸引 |
| 酒精灯 | 30 | 5 | 黑色 | 能 |
| 酒精喷灯 | 30 | 1 | 黑色 | 能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4、NaOH、NaNO3都是强电解质 | B. | Na2O、Al2O3、Fe2O3都是碱性氧化物 | ||
| C. | 铝土矿、小苏打都是混合物 | D. | 烧碱、纯碱、熟石灰都是碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCL(aq)$\stackrel{CO_{2}}{→}$NaHCO3(s)$\stackrel{△}{→}$NaCO3(s) | |
| B. | FeSz$→_{燃烧}^{O_{2}}$SO2$\stackrel{H_{2}O}{→}$H2SO4 | |
| C. | SiO2$\stackrel{HCl(aq)}{→}$SiCl4$→_{高温}^{H_{2}}$Si | |
| D. | N2$→_{高温、高压、催化剂}^{H_{2}}$NH3$\stackrel{HCl(aq)}{→}$NH4Cl(aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X单质与M单质不能直接化合 | |
| B. | Y的合金可用作航空航天飞行器材料 | |
| C. | M简单离子半径大于Y2+的半径 | |
| D. | X和Z的气态氢化物,前者更稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合物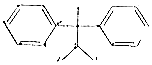 是苯的同系物 是苯的同系物 | |
| B. | 有机物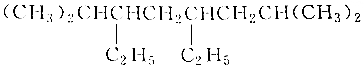 的系统名称是2-甲基-4-乙基-6-异丙基辛烷 的系统名称是2-甲基-4-乙基-6-异丙基辛烷 | |
| C. | C4H8的同分异构体只有3种 | |
| D. | 液化石油气的主要成分是烃,它是一种清洁燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温时,0.1 mol•L-1某一元酸在水中有0.1%电离,此酸的电离平衡常数约为1×10-7 | |
| B. | 反应CO(g)+3H2(g)=CH4(g)+H2O(g)一定条件下可自发进行,则该反应的△H>0 | |
| C. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 | |
| D. | 为减小中和滴定误差,锥形瓶和滴定管必须洗净并润洗后才能使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
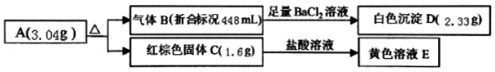
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石英坩埚耐高温,可用来加热熔化烧碱、纯碱等固体 | |
| B. | Al具有良好的延展性和抗腐蚀性,常用铝箔包装物品 | |
| C. | 浓H2SO4溶液能使蛋白质发生盐析,可用于杀菌消毒 | |
| D. | 铜的金属活动性比铁的弱,可在海外轮外壳上装若干铜块以减缓其腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com