
有A、B、C三种晶体,分别由H、C、Na、Cl四种元素中的一种或几种组成,对这三种晶体进行实验,结果如表:
| 序号 | 熔点/℃ | 硬度 | 水溶性 | 导电性 | 水溶液与Ag+反应 |
| A | 811 | 较大 | 易溶 | 水溶液或熔融导电 | 白色沉淀 |
| B | 3 500 | 很大 | 不溶 | 不导电 | 不反应 |
| C | -114.2 | 很小 | 易溶 | 液态不导电 | 白色沉淀 |
(1)晶体的化学式分别为A______________、B________________、C____________。
(2)晶体的类型分别是A______________、B_________________、C____________。
(3)晶体中微粒间作用力分别是A________、B__________________、C________。
科目:高中化学 来源: 题型:
下图是检验某无色气体A是SO2和CO2的混合气体的装置图,按要求回答下列问题。

(1)B中加入的试剂是________,作用是____________________________________________。
(2)C中加入的试剂是__________,作用是_______________________________________。
(3)D中加入的试剂是________,作用是_________________________________________。
(4)实验时,C中应观察到的现象是_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
由下列5种基团中的2个不同基团两两组合,形成的有机物能与NaHCO3溶液反应的有( )
①—OH ②—CH3 ③—COOH ④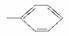 ⑤—CHO
⑤—CHO
A.2种 B.3种 C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的打“√”,错误的打“×”
(1)在晶体中只要有阴离子就一定有阳离子( )
(2)在晶体中只要有阳离子就一定有阴离子( )
(3)原子晶体的熔点一定比金属晶体的高( )
(4)分子晶体的熔点一定比金属晶体的低( )
(5)离子晶体一定都含有金属元素( )
(6)金属元素和非金属元素组成的晶体不一定是离子晶体( )
查看答案和解析>>
科目:高中化学 来源: 题型:
下列排列方式中,A.ABCABCABC B.ABABABABAB C.ABBAABBA D.ABCCBAABCCBA,属于镁型堆积方式的是____________;属于铜型堆积方式的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用晶体的X射线衍射法对Cu的测定得到以下结果:Cu的晶胞为

面心立方最密堆积(如右图),已知该晶体的密度为9.00 g·cm-3,晶胞中该原子的配位数为________;Cu的原子半径为________cm(阿伏加德罗常数为NA,要求列式计算)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.由于铵盐中是有离子键构成的,因而化学性质相当稳定
B.分子晶体中都存在分子间作用力,但可能不存在共价键
C.在常见的四种晶体类型中,都有“原子(离子)半径越大,物质熔点越低”的规律
D.常温下为气态或液态的物质,其固态时一定会形成分子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F、G、L、I九种主族元素分别位于三个不同的短周期,它们的原子序数依次增大,其中B、C、D位于同一周期,A与E、B与G、D与L分别位于同一主族,C、D、F三种元素的原子序数之和为28,F的质子数比D多5,D的最外层电子数是F最外层电子数的2倍,C和D的最外层电子数之和为11。请回答下列问题:
(1)以上元素中非金属所形成的最简单气态氢化物稳定性最弱的是(填化学式)__________________________,E、F、L所形成的简单离子的半径由大到小的顺序为(用离子符号表示)____________。
(2)L、I两元素可按原子个数比1∶1组成化合物X,化合物X中各原子均满足8电子的稳定结构,则X的电子式为__________________________________________。
(3)固体化合物E2D2投入到化合物E2L的水溶液中,只观察到有沉淀产生,写出该反应的离子方程式:_______________________。
(4)由A、B、C、D按原子个数比4∶1∶1∶2形成一种化合物Y,则Y的化学式为________________________,向Y中加足量稀硫酸后,再加高锰酸钾溶液,高锰酸钾溶液褪色。写出使高锰酸钾溶液褪色的反应的离子方程式:____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com