
将FeSO4·a(NH4)2SO4·bH2O的晶体9.6g与过量的氯化钡溶液反应,生成11.417gBaSO4;然后加入足量浓NaOH溶液并加热,产生的氨气用100ml 1mol/L盐酸吸收,剩余的盐酸再用2mol/LNaOH溶液中和,需NaOH溶液25.5ml。则
(1)9.6g晶体中SO42—离子的物质的量是_________________________
(2)晶体化学式中a、b的值是(均取整数):a=________;b=____________
科目:高中化学 来源: 题型:阅读理解
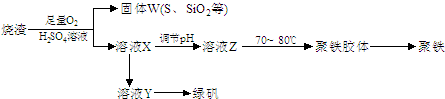
| ||
| ||
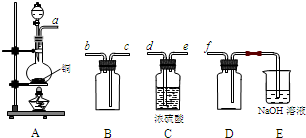
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| [O2][H2]2 |
| [H2O]2 |
| [O2][H2]2 |
| [H2O]2 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
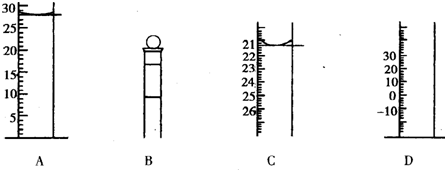
查看答案和解析>>
科目:高中化学 来源: 题型:
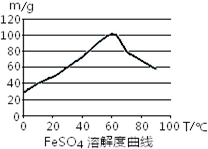 铁盐、亚铁盐在工农业生产、生活、污水处理等方面有着极其广泛的应用.
铁盐、亚铁盐在工农业生产、生活、污水处理等方面有着极其广泛的应用.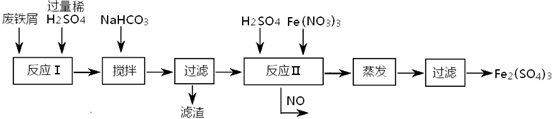
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 | 4.7 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 | 6.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com