
【题目】NaCl是一种化工原料,可以制备一系列物质(如图所示).下列说法正确的是( ) 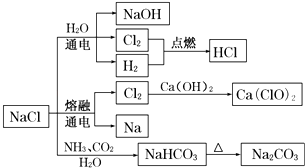
A.25℃,NaHCO3在水中的溶解度比Na2CO3的大
B.NaHCO3 受热分解的方程式为:2NaHCO3 ![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.电解饱和氯化钠溶液的方程式为:2NaCl ![]() 2Na+Cl2↑
2Na+Cl2↑
D.图中所示转化反应都是氧化还原反应
科目:高中化学 来源: 题型:
【题目】给定条件下,下列选项中所示的物质间转化均能通过一步反应实现的是( )
A.0.1 mol?L﹣1 HC1 ![]() ?C12
?C12 ![]() ?Ca(ClO)2(aq)
?Ca(ClO)2(aq)
B.Al3+ ![]() ?A1O2﹣
?A1O2﹣ ![]() ?Al(OH)3
?Al(OH)3
C.A1 ![]() ?NaA1O2(aq)
?NaA1O2(aq) ![]() ?NaAlO2(s)
?NaAlO2(s)
D.MgO(s) ![]() ?Mg(NO3)2(aq)
?Mg(NO3)2(aq) ![]() ?Mg(s)
?Mg(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据图中氮元素及其化合物的转化关系,判断下列说法不正确的是( ) 
A.X是N2O5
B.可用排空气法收集NO气体
C.工业上以NH3、空气、水为原料生产硝酸
D.由NH3→N2 , 从原理上看,NH3可与NO2反应实现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以Al和不同的铜盐溶液间的反应为实验对象,探索Al与不同铜盐溶液反应的多样性.
实验 | 向试管中加入2ml溶液 | 实验现象 |
| 实验Ⅰ:0.5mol/LCuCl2溶液 | 15s:大量气泡且有红色物质析出 |
实验Ⅱ:0.5mol/LCuSO4溶液 | 15s 无明显现象 |
(1)对实验Ⅰ进行研究②④ ①实验Ⅰ中生成红色物质的离子方程式为:
②经检验实验Ⅰ中产生的气体为氢气,用离子方程式解释溶液中存在H+的原因:
③请写出60s后反应进一步加快可能的原因(写出两条)
(2)对实验Ⅱ进行研究 实验Ⅱ反应明显比实验Ⅰ缓慢,说明Al与不同的铜盐溶液反应呈现多样性,其原因可能有:
假设一:SO42﹣对Al与Cu2+的置换反应存在一定的抑制作用.
假设二:
(3)为进一步研究上述假设,设计如下实验:
实验 | 向试管中加入2mL溶液 | 实验现象 |
| 实验Ⅲ:0.5mol/LCuCl2溶液+1g Na2SO4固体 | 加入 Na2SO4固体后速率几乎不变,仍有大量气泡产生,红色物质生成且剧烈放热,铝片反应完全,溶液沸腾 |
实验Ⅳ:0.5mol/L CuCl2溶液+5g Na2SO4固体 | 加入Na2SO4固体后速率几乎不变,仍有大量气泡产生,红色物质生成且剧烈放热,铝片反应完全,溶液沸腾 | |
实验Ⅴ:0.5mol/LCuSO4溶液+0.02mol NaCl固体 | 未加入 NaCl固体前几乎没现象,加入后,铝片表面迅速产生大量气体和红色物质,溶液温度上升至沸腾,铝反应完全 | |
实验Ⅵ:0.5mol/LCuSO4溶液+NH4Cl固体 | 未加入 NH4Cl固体前几乎没现象,加入后,铝片表面迅速产生大量气体和红色物质,溶液温度上升至沸腾,铝反应完全 |
实验Ⅵ的设计目的是:
其中,实验Ⅰ与实验Ⅲ、Ⅳ做对比,结论为:
其中,实验Ⅱ与实验Ⅴ、Ⅵ做对比,结论为:
(4)请设计实验证明Cl﹣对Al与H+的反应同样起到相似的作用:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4反应中,被氧化的P原子与被还原的P原子个数比是 ( )
A. 11:5 B. 5:6 C. 6:5 D. 11:6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应路线及所给信息,回答下列问题:

A在氧气中充分燃烧可以产生88 g CO2和45 g H2O。A的分子式是_______。
(2)B和C均为一氯代烃,它们的名称(系统命名)分别为_________________。
(3)D的结构简式________________,D中碳原子是否都处于同一平面?________。
(4)E的同分异构体的结构简式是___________________________。
(5)①、②、③的反应类型依次是_________________________。
(6)写出②、③的反应化学方程式_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com