
已知可逆反应温度为T0时,在容积固定的密闭容器中发生X(g)+Y(g) Z(g)(未配平)反应,各物质浓度随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应;Z的浓度随时间变化的关系如图b所示。下列叙述正确的是( )
Z(g)(未配平)反应,各物质浓度随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应;Z的浓度随时间变化的关系如图b所示。下列叙述正确的是( )

A.发生反应时,各物质的反应速率大小关系为v(X)=v(Y)=2v(Z)
B.图a中反应达到平衡时,Y的转化率为37.5%
C.T0时,该反应的平衡常数为33.3 D.该反应正反应的反应热ΔH<0
科目:高中化学 来源: 题型:
化学已经渗透到人类生活的各个方面,下列说法不正确的是
A. 食盐可作氯碱工业的原料
B. 碘酒是指单质碘的乙醇溶液
C. 大量使用化肥和农药,以提高农作物产量,符合绿色化学的原则
D. 低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,减少温室气体的排放
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D是四种常见单质,其对应元素的原子序数依次增大,其中B、D属于常见金属,J是一种黑色固体,I的浓溶液具有还原性,A~I均为中学化学常见物质,它们之间的转化关系如下图所示。(部分生成物和反应条件已略去)
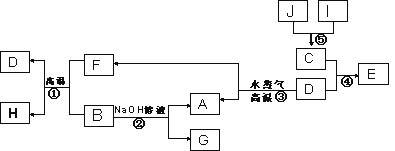
请回答下列问题:
(1) 写出组成物质D的元素在周期表中的位置:___________________。
(2) ①写出反应①的化学方程式:______________________________。
②由E的饱和溶液可以制得胶体,用化学方程式表示该过程的原理是_______________。
③写出反应②的离子方程式_________________________________。
(3) 已知G的水溶液显碱性,其原因是(用离子方程式表示)_________。
(4) J在H2O2分解反应中作催化剂。若将适量J加入酸化的H2O2溶液中,J溶解生成它的+2价离子,该反应的离子方程式是___________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20.0%,与反应前的体积相比,反应后体积缩小的百分率是( )
A.16.7% B.20.0% C.80.0% D.83.3%
查看答案和解析>>
科目:高中化学 来源: 题型:
1)反应aA(g)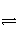
 bB(g)+cC(g)在一容积不变的容器内进行,反应达到平衡后(以下填“增大”、“减小”或“不变”):
bB(g)+cC(g)在一容积不变的容器内进行,反应达到平衡后(以下填“增大”、“减小”或“不变”):
①若a=b+c,增大A的浓度,A的转化率________。
②若a>b+c,增大A的浓度,A的转化率________。
(2)若反应aA(g)+bB(g)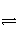
 cC(g)+dD(g),容器体积固定不变,且起始时A与B的物质的量之比为a∶b。
cC(g)+dD(g),容器体积固定不变,且起始时A与B的物质的量之比为a∶b。
①平衡时A与B的转化率之比是________。
②若增大A的浓度,则A的转化率________。
③若同时同等倍数地增大A、B的浓度,则a+b与c+d满足什么关系时,A与B的转化率同时增大?a+b______c+d(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
过碳酸钠(2Na2CO3·3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂。某兴趣小组制备过碳酸钠的实验方案和装置示意图如下:

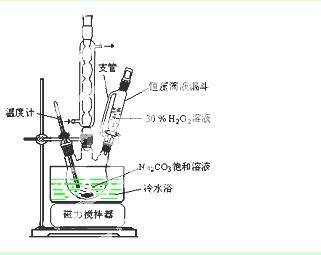
已知:主反应:2Na2CO3 (aq) + 3H2O2 (aq)  2Na2CO3·3H2O2 (s) ΔH < 0
2Na2CO3·3H2O2 (s) ΔH < 0
副反应:2H2O2 = 2H2O + O2↑,50℃时2Na2CO3·3H2O2 (s) 开始分解
请回答下列问题:
(1)步骤①的关键是控制温度,原因是 ,其措施有 、 和 。
(2)在滤液X中加入适量NaCl固体可析出过碳酸钠,原因是 。
(3)步骤③中选用无水乙醇洗涤产品的目的是 。
(4)下列物质中,会引起过碳酸钠失效的有 。
A.NaHCO3 B.MnO2 C.Na2SiO3 D.Na2SO3
(5)过碳酸钠产品中往往含有少量碳酸钠,可用重量法测定过碳酸钠的质量分数;其操作步骤:取样 品溶解→加入BaCl2溶液→过滤→洗涤→干燥→称量。需要直接测定的物理量有: 样品的质量m1g、沉淀的质量m2g(用字 母表示并注明其含义)。产品中过碳酸钠质量分数的表达式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( ) 
A. 的命名为:2-甲基-1-丙醇
B.软脂酸和油酸互为同系物
C.聚乙烯能使溴水褪色
D.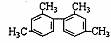 分子中至少有11个碳原子处于同一平面
分子中至少有11个碳原子处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列几种物质的熔点和沸点数据,判断下列有关说法中,错误的是( )。
| NaCl | MgCl2 | AlCl3 | SiCl4 | 单质B | |
| 熔点/℃ | 810 | 710 | 190 | -68 | 2 300 |
| 沸点/℃ | 1 465 | 1 418 | 182.7 | 57 | 2 500 |
注:AlCl3熔点在2.02×105 Pa条件下测定。
A.SiCl4是分子晶体
B.单质B是原子晶体
C.AlCl3加热能升华
D.MgCl2所含离子键的强度比NaCl大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com