
分析 (1)化学键是构成物质的重要方式之一,特殊的物质不存在任何化学键,如Ar等单原子分子;离子化合物中可能含有共价键,共价化合物中一定不含离子键;
(2)同素异形体的概念:由同种元素组成的结构性质不同的单质;同位素的概念:质子数相同,中子数不同的同种元素的不同核素;
(3)甲醇燃料电池,甲醇在负极失电子发生氧化反应.
解答 解:(1)CO2和HCl中,C和O、H和Cl都是以共价键相结合,故只存在共价键的是②③;
K2S中,K+与S2-以离子键相结合,故只存在离子键的是⑤;
NaOH中,Na+与OH-以离子键相结合,O与H之间是共价键,故既存在共价键又存在离子键的是④;
Ar是单原子分子,不存在任何化学键,故不存在化学键的是①,
故答案为:②③;⑤;④;①;
(2)①H2O和D2O,都是由氢氧元素组成的水,属于同种物质;
②质子数相同都是6,中子数不同分别是6、7,互为同位素;
③是由氧元素组成的两种不同单质,互为同素异形体;
④是由H元素组成的同种单质;
故答案为:②;③;
(3)甲醇燃料电池,甲醇在负极失电子发生氧化反应,电极反应式为:CH3OH+8OH--6e-=CO32-+6H2O,故答案为:CH3OH+8OH--6e-=CO32-+6H2O.
点评 本题考查了同位素、同素异形体、同分异构体、同系物的概念本、对物质中的化学键的认识,并不是所有的物质都含有化学键,稀有气体中不含有任何化学键.


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:实验题
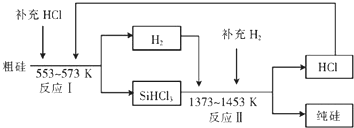
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
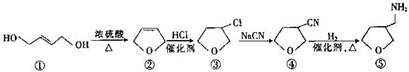
| A. | 有机物①与乙烯互为同系物 | |
| B. | 有机物③转化为有机物④的反应属于加成反应 | |
| C. | 有机物④转化为有机物⑤的反应中反应物的物质的量之比为1:1 | |
| D. | 含有一个四元环,且能与金属钠反应的有机物③的同分异构体(不考虑立体异构)有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化 | |
| B. | NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道 | |
| C. | NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强 | |
| D. | 甲烷中心原子的价电子全部成键且成键的对象相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 64种 | B. | 8种 | C. | 32种 | D. | 16种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 定容时观察液面俯视 | B. | 未冷却直接转移溶液 | ||
| C. | 有少量NaOH溶液残留在烧杯中 | D. | 容量瓶中原来有少量蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 量筒的“0”在下方 | B. | 滴定管的“0”在上方 | ||
| C. | 移液管的“0”在尖嘴处 | D. | 托盘天平的“0”在刻度盘的中央 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
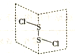 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示.
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com