
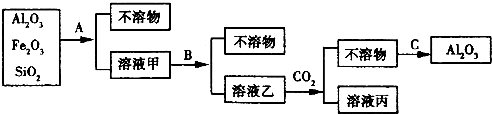


科目:高中化学 来源: 题型:
| Al2O3 | Fe2O3 | Na2O | |
| 铝土矿 | 55% | 16% | 0% |
| 赤泥 | 15% | 48% | 8% |
查看答案和解析>>
科目:高中化学 来源: 题型:
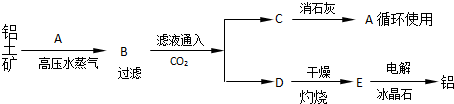
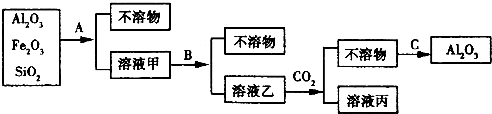
工业上制取铝的流程如下:
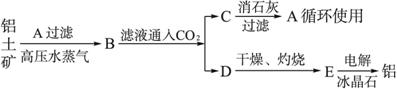
注:冰晶石的作用是使E在较低温度下熔化。
(1)试写出下列物质的化学式:
A____________,B____________,C____________,?D____________?,E____________。
(2)在用此法制取铝时,分析铝土矿和赤泥(提取Al2O3之后的残渣)所得数据如下:
| Al2O3 | Fe2O3 | Na2O | 铝土矿 |
| 55% | 16% | 0% | 赤泥 |
| 15% | 48% | 8% |
试求制取1 t Al2O3所需铝矾土和苛性钠的质量。
查看答案和解析>>
科目:高中化学 来源:2013届辽宁省铁岭市六校协作高三第一次联合考试化学试卷(带解析) 题型:填空题
(15分)工业上制取铝的流程如下: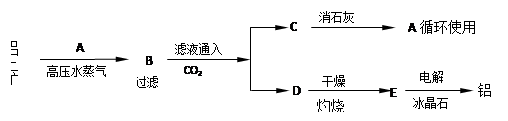
注:冰晶石的作用是使E在较低温度下熔化。
(1)试写出下列物质的化学式:
A ,B ,C ,D ,E 。
(2)在用此法制取铝时,分析铝土矿和赤泥(提取Al2O3之后的残渣)所得数据如下:
| | Al2O3 | Fe2O3 | Na2O |
| 铝土矿 | 55% | 16% | 0% |
| 赤泥 | 15% | 48% | 8% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com