
下列溶液一定呈中性的是
A.pH=7的溶液 B.c(H+)=c(OH-)=10-6mol/L的溶液
C.使酚酞试液呈无色的溶液 D.由强酸与强碱等物质的量反应得到的溶液
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
已知金属活动相差越大,形成原电池时越容易放电。请根据如图装置,回答下列问题:

(1)各装置名称是:A池________,B池______,C池________。
(2)写出电极上发生的反应:①_____________,③___________,⑤_____________。
(3)当电路上有2 mol电子流过时,①极上质量变化______g,⑥极上质量变化______g。
(4)反应进行一段时间后,A、B、C三池中电解质溶液浓度不变的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。
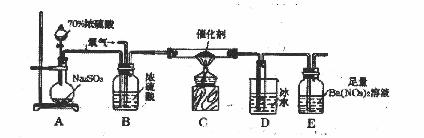
(1)实验室用上述装置测定SO2催化氧化为SO3的转化率。(已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响。)
①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作: 。
②实验过程中,需要通入氧气。试写出一个用如图所示装置制取氧气的化学方程式: 。
③当停止通入SO2熄灭酒精灯后,需要继续通一段时间的氧气,其目的是: 。
④实验结束后,若装置D增加的质量为mg,装置E中产生白色沉淀的质量为ng,则此
条件下二氧化硫的转化率是 (用含字母的代数式表示,不用化简)。
(2)某学习小组设计用如图装置验证二氧化硫的化学性质。
①能说明二氧化硫具有氧化性的实验现象为:
。
 ②为验证二氧化硫的还原性,充分反应后,取试管b
②为验证二氧化硫的还原性,充分反应后,取试管b
中的溶液分三份,分别进行如下实验。
方案I:向第一份溶液中加入AgNO3溶液,有白色沉
淀生成。
方案II:向第二份溶液中加入品红溶液,红色褪去。
方案III:向第三份溶液中加入BaC12溶液,产生白色沉淀
上述方案中合理的是 (填“I”、“II”、或“III”);
试管b发生反应的离子方程式: 。
③当通入二氧化硫至试管c中溶液显中性时,该溶液中
c(Na+)= 用含硫微粒浓度的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活密切相关。下列情况会对人体健康造成较大危害的是
A.用于消化道检查的钡餐(硫酸钡)
B.用SO2漂白食品
C.用食醋清洗热水瓶胆内壁附着的水垢(CaCO3)
D.用小苏打(NaHCO3)发酵面团制作馒头
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是
A.强电解质溶液的导电能力一定比弱电解质溶液的强
B.离子化合物中可能有共价键,共价化合物中肯定没有离子键
C.强电解质都是可溶性化合物,弱电解质都是难溶性化合物
D.NaCl晶体不导电是由于NaCl晶体中不存在离子
查看答案和解析>>
科目:高中化学 来源: 题型:
对于常温下pH=3的乙酸溶液,下列说法正确的是
A.c(H+)=c(CH3COO-)+c(OH-)
B.加水稀释到原体积的10倍后溶液pH变为4
C.加入少量乙酸钠固体,溶液pH降低
D.与等体积pH=11的NaOH溶液混合后所得溶液中:c(Na+)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在5 mL 0.1 mol/L的KCl溶液中,加入5 mL 0.1 mol/L的AgNO3溶液,可观察到____________,此反应的离子方程式为_____________________。
将此混合液过滤,滤渣加入5 mL 0.1 mol/L的KI溶液,搅拌,可观察到________________________,反应的离子方程式为_____________________。
(2)对于Ag2S(s) 2Ag+(aq)+S2-(aq),其Ksp的表达式为_____________________。
2Ag+(aq)+S2-(aq),其Ksp的表达式为_____________________。
(3)下列说法不正确的是________。
A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小
B.对于Al(OH)3(s)  Al(OH)3(aq)
Al(OH)3(aq)  Al3++3OH-,前者为溶解平衡,后者为电离平衡
Al3++3OH-,前者为溶解平衡,后者为电离平衡
C.物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的
D.沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全
E.用OH-除去溶液中的Mg2+比用CO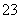 效果好,说明Mg(OH)2的溶解度比MgCO3大
效果好,说明Mg(OH)2的溶解度比MgCO3大
(4)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是______。
A. KMnO4 B. H2O2 C. Cl2 水 D. HNO3
然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的________。
A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既是氧化还原反应,又是吸热反应的是
A.灼热的炭与CO2反应 B.Ba(OH)2·8H2O与NH4Cl的反应
C. 铝片与稀硫酸反应 D.甲烷在O2中的燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)按系统命名法命名.
①有机物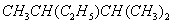 的名称是 。
的名称是 。
(2)写出下列各种有机物的结构简式
①2,3-二甲基-4-乙基已烷 ;
②支链只有一个乙基且式量最小的烷烃 ;
③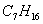 的同分异构体中具有“手性碳原子”的有 种,写出其中一种的名称 。
的同分异构体中具有“手性碳原子”的有 种,写出其中一种的名称 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com