
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池,如图所示。
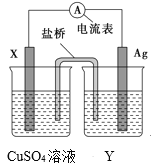
请回答下列问题:
(1)电极X的材料是___;电解质溶液Y是___。
(2)银电极为电池的___极,发生的电极反应为___。X电极上发生的电极反应为___。
(3)外电路中的电子是从____极流向___极。
【答案】铜(或Cu) AgNO3溶液 正 Ag++e=Ag Cu2e=Cu2+ 负(或Cu) 正(或Ag)
【解析】
原电池中负极上发生氧化反应,正极上发生还原反应,盐桥起到形成闭合回路、平衡电荷的作用。由总反应方程式可知电极X的材料是铜,发生氧化反应,电解质溶液Y是可溶性银盐溶液,常用硝酸银溶液。电极反应式表示为负极:Cu2e=Cu2+,正极:Ag++e=Ag,电子由负极(或Cu)出发,经外电路流向正极(或Ag)。
(1)原电池中负极上发生氧化反应,正极上发生还原反应,盐桥起到形成闭合回路、平衡电荷的作用。由总反应方程式可知电极X的材料是铜,发生氧化反应,电解质溶液Y是可溶性银盐溶液,常用硝酸银溶液。故正极是铜,电解质溶液Y是硝酸银溶液;
(2)电极反应式表示为负极:Cu2e=Cu2+,正极:Ag++e=Ag;
(3)电子由负极(或Cu)出发,经外电路流向正极(或Ag)。


科目:高中化学 来源: 题型:
【题目】在一定温度下,将2molA和2molB两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g) ![]() xC(g)+2D(g),2min后反应达平衡状态,生成0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)+2D(g),2min后反应达平衡状态,生成0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x值等于____;
(2)A的转化率为______;
(3)生成D的反应速率为___________;
(4)如果增大体系的压强,则平衡体系中C的质量分数_____(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.![]()
![]() ,结论:
,结论:![]() 的燃烧热为
的燃烧热为![]()
B.稀溶液中有![]()
![]() ,结论:将盐酸与氨水的稀溶液混合后,若生成
,结论:将盐酸与氨水的稀溶液混合后,若生成![]() ,则会放出
,则会放出![]() 的能量
的能量
C.相同条件下,如果![]() 氢原子所具有的能量为
氢原子所具有的能量为![]() ,
,![]() 氢分子所具有的能量为
氢分子所具有的能量为![]() ,则
,则![]()
D.![]() 气态乙硼烷
气态乙硼烷![]() 在
在![]() 中完全燃烧生成固态
中完全燃烧生成固态![]() 和液态水,同时放出
和液态水,同时放出![]() 的热量,该反应的热化学方程式为
的热量,该反应的热化学方程式为![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有4种混合溶液,分别由等体积 ![]() 的两种溶液混合而成:
的两种溶液混合而成:![]() 与
与![]() 混合溶液呈中性
混合溶液呈中性![]() 与
与![]() 与
与![]() 与
与![]() 混合溶液呈碱性
混合溶液呈碱性![]() 。下列各项排序正确的是
。下列各项排序正确的是![]()
A.pH:![]()
B.溶液中![]() :
:![]()
C.![]() :
:![]()
D.![]() :
:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关溶液![]() 室温下
室温下![]() 的说法正确的是
的说法正确的是![]()
A.![]() 和
和![]() 形成的混合溶液中:
形成的混合溶液中:![]()
B.![]() 溶液中通入
溶液中通入![]() 至溶液
至溶液![]() :
:![]()
C.物质的量浓度相等的![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液中,
溶液中,![]() 的大小关系:
的大小关系:![]()
D.![]() 溶液中通入HCl至溶液
溶液中通入HCl至溶液![]() :
:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式与所述事实相符且正确的是( )
A.用惰性电极电解熔融氯化钠:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-=Mn2++Cl2↑+2H2O
C.向Na[Al(OH)4]溶液中通入过量CO2制Al(OH)3:[Al(OH)4]-+CO2=Al(OH)3↓+HCO3-
D.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1 L浓度为0.4 mol·L-1的乙醇酸[CH2(OH)COOH]溶液中加入8 g NaOH固体得到X溶液,将X溶液平均分成两等份,一份通入HCl气体,得到溶液Y,另一份加入NaOH固体得到溶液Z,溶液Y、Z的pH随所加物质的物质的量的变化情况如图所示(体积变化忽略不计)。下列说法正确的是

A. c点对应曲线代表的是加入NaOH的曲线
B. 溶液中水的电离程度:c>b
C. a点:c[CH2(OH)COO-]>c(Na+)>c(H+)>c(OH-)
D. 稀释Y溶液后,溶液中![]() 变大
变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿素[CO(NH2)2]作为一种中性肥料,适用于各种土壤和植物。它易保存,使用方便,对土壤的破坏作用小,是目前使用量较大的一种高效化肥,同时也是一种化工 原料。
(1)以尿素为原料在一定条件下发生反应:CO(NH2)2(s) + H2O(l)![]() 2NH3(g)+CO2(g),△H = +133.6 kJ·mol-1 。在一定条件下可将氮的氧化物还原为氮气(能量示意图如下),结合相关信息写出尿素还原 NO(g)的热化学方程式是____。
2NH3(g)+CO2(g),△H = +133.6 kJ·mol-1 。在一定条件下可将氮的氧化物还原为氮气(能量示意图如下),结合相关信息写出尿素还原 NO(g)的热化学方程式是____。
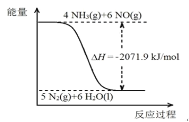
(2)恒温恒容密闭容器中,下列可以证明工业合成氨气反应达到平衡的标志是_______(填序号)。
A.N2、H2 和 NH3 的浓度相等
B.1 mol 氮氮三键断裂同时 6mol N-H键断裂
C.混合气体的密度保持不变
D.混合气体的平均相对分子质量不再改变
(3)工业上生产尿素的化学方程式:2NH3(g)+CO2(g)![]() CO( NH2)2( s)+H2O(1)。
CO( NH2)2( s)+H2O(1)。
①在一定温度和压强下,设原料气体中的氨炭比:n(NH3)/n(CO2) = x。下图是氨炭比(x)与 CO2平衡转化率[α(CO2)]的关系。α(CO2)随x的增大而增大的原因是:___________________________________。
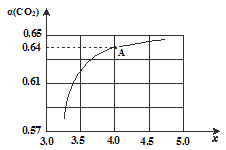
②图中A点处,NH3的平衡转化率为____________。
③在T℃,体积为10L的密闭容器中,通入6 mol NH3和3 mol CO2,反应经5 min达到平衡时n(NH3) =2mol,反应开始到平衡反应速率v(CO2)= ___________________。平衡常数 K=___________________(填计算结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 在玻璃工业中常用作澄清剂和脱色剂,工业上采用酸性高浓度含砷废水
在玻璃工业中常用作澄清剂和脱色剂,工业上采用酸性高浓度含砷废水![]() 主要以
主要以![]() 形式存在
形式存在![]() 提取
提取![]() 的工艺流程如下:
的工艺流程如下:
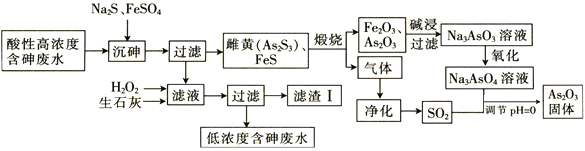
回答下列问题:
![]() 上述流程的__________过程中由于条件的原因,造成生成物中混有
上述流程的__________过程中由于条件的原因,造成生成物中混有![]() ,为证明
,为证明![]() 的存在,可利用
的存在,可利用![]() 具有____________性的这一物理性质。
具有____________性的这一物理性质。
![]() 调节
调节![]() 时,由
时,由![]() 制备
制备![]() 的离子方程式为_____________________________。
的离子方程式为_____________________________。
![]() 常温下,用NaOH溶液滴定
常温下,用NaOH溶液滴定![]() 时,各种微粒的物质的量分数随pH的变化曲线如图所示:
时,各种微粒的物质的量分数随pH的变化曲线如图所示:
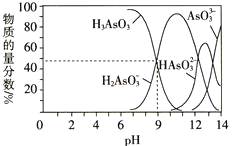
![]() AsO
AsO![]() 为________元________
为________元________![]() 填“强”或“弱”
填“强”或“弱”![]() 酸。
酸。
![]() 由7调节至10的过程中发生反应的离子方程式为____________________________。
由7调节至10的过程中发生反应的离子方程式为____________________________。 ![]() 的一级电离平衡常数
的一级电离平衡常数![]() _______。
_______。
![]() 滤渣Ⅰ中含有
滤渣Ⅰ中含有![]() 、
、![]() 、
、![]() 和_______________
和_______________![]() 填化学式
填化学式![]() ;已知
;已知
![]() ,含砷污染物允许排放标准为不大于
,含砷污染物允许排放标准为不大于![]() 。若低浓度含砷废水
。若低浓度含砷废水![]() 假设砷均以
假设砷均以![]() 形式存在
形式存在![]() 中
中![]() 的浓度为
的浓度为![]() ,则低浓度含砷废水中
,则低浓度含砷废水中![]() 的浓度为_________
的浓度为_________![]() ,________
,________![]() 填“符合”或“不符合”
填“符合”或“不符合”![]() 排放标准。
排放标准。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com