
| A. | N2O | B. | N2 | C. | NO | D. | NO2 |
分析 由信息“用25.00mL0.049mol•L-1的羟胺的酸性溶液跟足量的Fe2(SO4)3溶液在煮沸条件下反应,生成Fe2+离子恰好与24.5mL0.020049mol•L-1 的酸性KMnO4溶液完全作用”可知,NH2OH失去电子数等于高锰酸钾得到电子数,以此来计算.
解答 解:由25.00mL 0.049mol/L的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.5mL0.020049mol•L-1 的KMnO4酸性溶液完全作用可知,
NH2OH失去电子数等于高锰酸钾得到电子数,
设羟胺的氧化产物中N元素的化合价为x,
由电子守恒可知,25.00mL×0.001L×0.049mol/L×(x+1)=24.50mL×0.001L×0.020049mol•L-1×(7-2),
解得x=1,羟胺的氧化产物是N2O,
故选A.
点评 本题考查氧化还原反应的计算,为高频考点,把握反应中电子守恒为解答的关键,注意从化合价变化角度及电子守恒分析,题目难度不大.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因为NH3的水溶液可以导电,所以NH3是电解质 | |
| B. | 因为O2可以与CO反应生成CO2,所以可以用O2除去CO2中的杂质CO | |
| C. | 因为液态HCl不导电,所以HCl是非电解质 | |
| D. | 因为氢氧化铁胶体具有吸附性,所以常用于净水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24 L 水中所含的电子数为NA | |
| B. | 常温常压下,16 g O3所含的原子数为NA | |
| C. | 0.1 mol Na2O2 晶体中所含的离子数为0.4NA | |
| D. | 1 mol Fe在氧气中充分燃烧失去的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
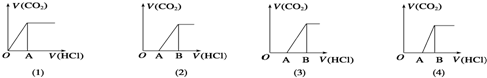
| A. | M中只有一种溶质的有 (1)和(3) | B. | M中有两种溶质的只有(2) | ||
| C. | (2)图显示M中c(NaHCO3)>c(Na2CO3) | D. | (4)图显示M中c(NaHCO3)>c(Na2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com