
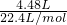 =0.2mol,气体分子与被还原的硝酸的关系式为
=0.2mol,气体分子与被还原的硝酸的关系式为 =0.2mol,则0.2molCu变成Cu2+失去的电子为0.2mol×2=0.4mol,
=0.2mol,则0.2molCu变成Cu2+失去的电子为0.2mol×2=0.4mol,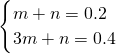 ,解得m=0.1mol,n=0.1mol,
,解得m=0.1mol,n=0.1mol,

科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述:
①我国科学家在世界上第一次人工合成结晶牛胰岛素;
②最早发现电子的是英国科学家道尔顿;
③测定有机化合物中碳、氢元素质量分数的方法最早由李比希提出;
④荷兰化学家范特霍夫提出碳原子成键的新解释,成功地解决了二取代甲烷只有一种结构的问题;
⑤首先在实验室合成尿素的是维勒,
其中正确的是
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com