
【题目】下列是某些元素基态原子的电子排布式,其中表示第三周期元素的是( )
A.1s22s1 B.1s22s22p5
C.1s22s22p63s2 D.1s22s22p63s23p64s1
科目:高中化学 来源: 题型:
【题目】氯贝特( )是临床上一种降脂抗血栓药物,它的一条合成路线如下:
)是临床上一种降脂抗血栓药物,它的一条合成路线如下:

提示:Ⅰ.图中部分反应条件及部分反应物、生成物已略去。
Ⅱ.
Ⅲ.![]()
⑴氯贝特的分子式为 。
⑵若8.8 g A与足量NaHCO3溶液反应生成2.24 L CO2(标准状况),且B的核磁共振氢谱有两个峰,则A的结构简式为 。(相对原子质量:H-1、C-12、O-16)
⑶要实现反应①所示的转化,加入下列物质不能达到目的的是 (填选项字母)。
a.Na b.NaOH c.NaHCO3 d.CH3COONa
⑷反应②的反应类型为 ,其产物甲有多种同分异构体,同时满足以下条件的所有甲的同分异构体有 种(不考虑立体异构)。
① 1,3,5-三取代苯;
② 属于酯类且既能与FeCl3溶液显紫色,又能发生银镜反应;
③ 1 mol该同分异构体最多能与3 mol NaOH反应。
⑸写出B与足量NaOH溶液反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.钠保存在煤油里的原因之一是它极易与氧气反应
B.铝在空气中很容易燃烧
C.镁表面的氧化膜疏松,不能保护内层金属
D.铝制容器能用来长期存放碱性食物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于消去反应的是 ( )
A. 乙烷与溴水的反应
B. 一氯甲烷与KOH的乙醇溶液混合加热
C. 氯苯与NaOH水溶液混合加热
D. 溴丙烷与KOH的乙醇溶液混合加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 处于下列状态的物质中:
①硫酸钡晶体 ②干冰 ③HCl气体 ④铜 ⑤蔗糖 ⑥熔融的硝酸钾 ⑧NaCl溶液 ⑨醋酸
(1)能导电的是(填序号,下同)______________________;
(2)属于弱电解质_______________;
(3)属于非电解质的是___________________________。
II.某消毒液的主要成分为NaClO(混有少量NaCl),请用相应的化学用语来解释下列事实。
(1)该消毒液可用NaOH 溶液吸收Cl2 制备,化学方程式为_______________________;
(2)该消毒液的pH 约为12,离子方程式为_______________________________________;
(3)向FeSO4溶液中滴入少量该消毒液,溶液变成棕黄色,反应的离子方程式为______________________________________;
(4)该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险。每产生1 mol Cl2(标准状况下),转移电子个数约为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示:
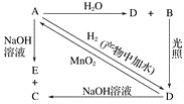
(1)请分别写出下列物质的化学式(如为溶液请填溶质的化学式):A________、B________、D________。
(2)写出下列反应的化学方程式或离子方程式(请注明反应条件):A+H2O(离子方程式):_________;A+NaOH(离子方程式):_______________;D→A(化学方程式):____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.氯水能导电,所以氯气是电解质
B.固体氯化钠不导电,但氯化钠是强电解质
C.BaSO4的水溶液不能导电,所以BaSO4属于非电解质
D.NH3溶于水能导电,所以NH3是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池构造如图所示,下列叙述正确的是:
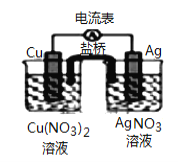
A. 原电池的总反应式为:Cu+2AgNO3 = 2Ag+Cu(NO3)2
B. 取出盐桥后,电流表的指针仍发生偏转
C. 外电路中每通过0.1 mol电子,铜的质量理论上减小6.4 g
D. 在外电路中,电子由银电极流向铜电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,在体积为2L的密闭容器中(容积不变)通人3mo1和1molB,发生反应3A(g)+B(g)xC(g);经过2min的时间该反应达到平衡状态(假设温度不变),剩余的B的物质的量为0.8mol并测得C的浓度为0.4 molL-1
请回答下列问题:
(1)整个反应过程中,B的平均反应速率为______________
(2)x=_______,平衡常数K=_______.
(3)如果向该平衡体系中通人少量氮气、增大反应体系的压强,那么化学平衡的移动方向是____________.
(4)若温度不变,再向原平衡混合物的容器中充人amolC在t℃时达到新的平衡,此时B的物质的量为nmol,则C的物质的量为_____(用含n的表达式表示),平衡常数K______(填“增大”“减小”或不变”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com