
 实验室采购了部分化学药品.如图是从化学试剂商店买回的硫酸试剂标签上的部分内容.下列说法正确的是( )
实验室采购了部分化学药品.如图是从化学试剂商店买回的硫酸试剂标签上的部分内容.下列说法正确的是( )| A. | 该硫酸的物质的量浓度为9.2mol•L-1 | |
| B. | 1molAl与足量的该硫酸反应产生3g氢气 | |
| C. | “化学纯”是指这种硫酸只含H2SO4和H2O分子 | |
| D. | 配制460mL2.3mol•L-1的稀硫酸需量取该硫酸62.5 mL |
分析 A.根据c=$\frac{1000ρω}{M}$计算浓度;
B.铝与浓硫酸常温下发生钝化,加热时生成二氧化硫和硫酸铝;
C.化学纯是指试剂纯度,与粒子的存在状态无关;
D.根据溶液稀释前后浓度不变分析.
解答 解:A.c=$\frac{1000ρω}{M}$=$\frac{1000×1.84g/mL×98%}{98g/mol}$=18.4mol/L,故A错误;
B.铝与浓硫酸常温下发生钝化,加热时生成二氧化硫和硫酸铝,不能生成氢气,故B错误;
C.化学纯是指试剂纯度,与粒子的存在状态无关,浓硫酸中还存在少量的氢离子、氢氧根离子以及硫酸根离子,故C错误;
D.配制460mL2.3mol•L-1的稀硫酸,应选取500mL容量瓶,故配制出500mL2.3mol•L-1的稀硫酸,根据溶液稀释前后浓度不变可知0.5L×2.3mol/L=V×18.4mol/L,解得V=62.5mL,故D正确.
故选D.
点评 本题考查浓硫酸的性质、物质的量浓度的计算以及溶液的配制等问题,侧重于学生的分析能力和计算能力的考查,难度不大,注意相关计算公式的运用.


科目:高中化学 来源: 题型:推断题
 无机物甲、乙、丙经一步反应的转化关系如图所示,其中部分反应物、生成物及反应条件已略去.
无机物甲、乙、丙经一步反应的转化关系如图所示,其中部分反应物、生成物及反应条件已略去.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 步骤①、③的操作分别是过滤、萃取分液 | |
| B. | 可用淀粉溶液检验步骤②的反应是否进行完全 | |
| C. | 步骤③中加入的有机溶剂是乙醇 | |
| D. | 步骤④的操作是过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2既是氧化产物又是还原产物 | |
| B. | CuFeS2既是氧化剂又是还原剂 | |
| C. | O2只做氧化剂 | |
| D. | 若有1mol O2参加反应,则反应中有4mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体形状改变且质量减少 | |
| B. | 晶体形状改变而质量不变 | |
| C. | 晶体形状和质量都不变 | |
| D. | 硫酸铜溶液的物质的量浓度有所增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1的NaOH溶液:K+、Na+、SO42-、CO32- | |
| B. | 0.1mol•L-1的Na2CO3溶液:K+、Ba+、NO32-、Cl- | |
| C. | 0.1mol•L-1的FeCl3溶液:K+、NH4+、I-、SCN- | |
| D. | c(H+)/c(OH-)=1×1014的溶液:Ca2+、Na+、ClO-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
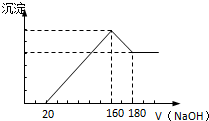 将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为2mol/L的NaOH溶液,生成的沉淀与加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)
将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为2mol/L的NaOH溶液,生成的沉淀与加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com