
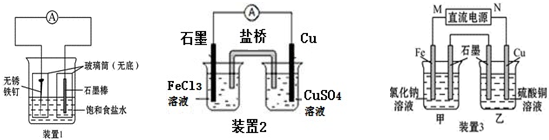
���� ��1��������������ʴ��������������Fe2+������������ԭ��Ӧ�������õ����ӱ���ԭ����OH-��
��2���γ�ԭ��أ��ܷ���ʽΪCu+2Fe3+=Cu2++2Fe2+�������ܷ���ʽ�жϣ�
��3������ձ��е��뼸�η�̪���۲쵽ʯī�缫�������ȱ�죬˵��ʯī������OH-��ӦΪ���ص���������MΪ������NΪ���������ձ�Ϊ�������ķ�Ӧ������������������������ͭ����ϵ缫����ʽ�����⣮
��� �⣺��1��������������ʴ������������ԭ��Ӧ�������õ����ӱ���ԭ����OH-���缫����ʽΪO2+2H2O+4e-�T4OH-��
�ʴ�Ϊ��O2+2H2O+4e-�T4OH-��
��2��ͭ�ɱ�Fe3++����������Cu+2Fe3+=Cu2++2Fe2+���γ�ԭ��ط�Ӧʱ��ͭΪ����������������Ӧ��ʯīΪ������������ӦΪFe3++e-=Fe2+��
�ʴ�Ϊ������ Fe3++e-=Fe2+��
��3�����ձ�Ϊ�������ķ�Ӧ������������������������ͭ��
������ձ��е��뼸�η�̪���۲쵽ʯī�缫�������ȱ�죬˵��ʯī������OH-��ӦΪ���ص���������MΪ������NΪ��������Ϊ����������Ȼ�����Һ������������ԭ��Ӧ�����������缫����ʽΪ2H++2e-�TH2����
�ʴ�Ϊ������ 2H2O+2e-=H2��+2OH-��2H++2e-�TH2����
�����ձ�Ϊ�������ķ�Ӧ������������������������ͭ����ⷽ��ʽΪ2Cu2++2H2O$\frac{\underline{\;���\;}}{\;}$2Cu+O2��+4H+��
�ʴ�Ϊ��2Cu2++2H2O$\frac{\underline{\;���\;}}{\;}$2Cu+O2��+4H+��
��ȡ��Cu�缫��ϴ�ӡ�����������缫����0.64g��������Cu�����ʵ���Ϊ$\frac{0.64g}{64g/mol}$=0.01mol��ת�Ƶĵ��ӵ����ʵ���Ϊ0.01mol��2=0.02mol��
���ձ��У���������������������������Ϊ������
2H2O+2e-�T2OH-+H2����
2mol 22.4L
0.02mol V
V=$\frac{22.4L��0.02mol}{2mol}$=0.224L����224mL��
�ʴ�Ϊ��224��
���� ���⿼��绯ѧ֪ʶ��Ϊ��Ƶ���㣬������ѧ���ķ��������������Ŀ��飬��Ŀ�Ѷ��еȣ�����ʱע��缫���жϺ͵缫��Ӧ����д��ע�����·�и��缫ת�Ƶĵ�����Ŀ��ȣ����÷�Ӧ�ķ���ʽ���㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | a��b | B�� | b��c | C�� | a��d | D�� | b��d |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Һ�� | B�� | Ư�� | C�� | ���� | D�� | �ơ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | I�͢� | B�� | I��IV | C�� | ��͢� | D�� | ���IV |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢܢ� | B�� | ֻ�Т٢ڢۢ� | C�� | ֻ�Т٢ڢ� | D�� | ֻ�Т٢ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���軯� | B�� | ������ | C�� | ���� | D�� | ���Ȼ�̼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ʵ��������һδ֪Ũ�ȵ�ϡ���ᣬijѧ����ʵ�����н��вⶨ����Ũ�ȵ�ʵ�飻�����������գ�
ʵ��������һδ֪Ũ�ȵ�ϡ���ᣬijѧ����ʵ�����н��вⶨ����Ũ�ȵ�ʵ�飻�����������գ�| �ζ����� | ��������������mL�� | ��NaOH��Һ��� | |
| �ζ�ǰ�Ŀ̶ȣ�mL�� | �ζ���Ŀ̶ȣ�mL�� | ||
| ��һ�� | 20.00 | 0.40 | 20.50 |
| �ڶ��� | 20.00 | 4.10 | 24.00 |
| ������ | 20.00 | 1.00 | 24.00 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
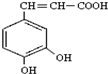 ��Ҳ��3��4-���ǻ���Ƥ�ᣬ��������������ҩ�У���Ұ���ܲ�����Ҷˮ�ա�����ľ���ĵȣ���������ֹѪ���ã��������ֹѪЧ���Ϻã����Խ�С��������ȡ���̵����Ч��
��Ҳ��3��4-���ǻ���Ƥ�ᣬ��������������ҩ�У���Ұ���ܲ�����Ҷˮ�ա�����ľ���ĵȣ���������ֹѪ���ã��������ֹѪЧ���Ϻã����Խ�С��������ȡ���̵����Ч�� ��д����������NaHCO3��Һ��Ӧ�ķ���ʽ����
��д����������NaHCO3��Һ��Ӧ�ķ���ʽ����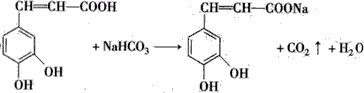 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com