
| A. | c(Na+)>c(HCO3-)>c(H+)>c(OH-) | B. | c(Na+)=c(HCO3-)+c(CO32-)+2c(H2CO3) | ||
| C. | c(H+)+c(H2CO3)=c(OH-) | D. | c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-) |
分析 A、在0.1mol/L的NaHCO3溶液中,HCO3-的水解大于其电离;
B、根据物料守恒来分析;
C、根据质子守恒来分析;
D、根据电荷守恒来分析.
解答 解:A、在0.1mol/L的NaHCO3溶液中,钠离子的浓度为0.1mol/L,而HCO3-既能水解又能电离,故c(Na+)>c(HCO3-),而HCO3-的水解大于其电离,故溶液显碱性,故有c(OH-)>c(H+),则有:c(Na+)>c(HCO3-)>c(OH-)>c(H+),故A错误;
B、HCO3-既能水解为H2CO3,又能电离为CO32-,根据物料守恒可知:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3),故B错误;
C、溶液中的氢离子来自于水的电离和HCO3-的电离,氢氧根均来自于水,而水电离出的氢离子和氢氧根的浓度相等,故根据质子守恒可知:c(H+)+c(H2CO3)=
c(OH-)+c(CO32-),故C错误;
D、任何溶液均显电中性,NaHCO3溶液中根据电荷守恒来列式可知:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),故D正确.
故选D.
点评 本题考查了盐溶液中的三个守恒的应用,难度不大,应注意基础的掌握.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 煤中含有苯、二甲苯等,因此可以通过煤的干馏得到,并将它们分离 | |
| B. | 酒精消毒原理是将病毒彻底氧化 | |
| C. | 绿色化学的核心是利用化学原理治理环境污染 | |
| D. | 麦芽糖的水解产物能发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸、碱、盐、氧化物在组成上的共同点是都含有非金属元素 | |
| B. | 只含有一种元素的物质都是纯净物 | |
| C. | 制糖工业中利用活性炭脱色制白糖的过程是物理变化 | |
| D. | 压强恒定时,气体在水中的溶解度随温度的升高而降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| B. | 已知S(s)+O2(g)═SO2(g)△H1;S(g)+O2(g)=SO2(g)△H2,则△H1>△H2 | |
| C. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ/mol,则氢气的燃烧热为241.8kJ/mol | |
| D. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3kJ/mol,则含20gNaOH的稀溶液与稀盐酸完全中和,中和热为28.65kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2,3-二甲基-3,3-二乙基戊烷 | B. | 2-甲基-3-乙基丁烷 | ||
| C. | 2,2-二甲基-2-丁醇 | D. | 2,3-二甲基-1-丁醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
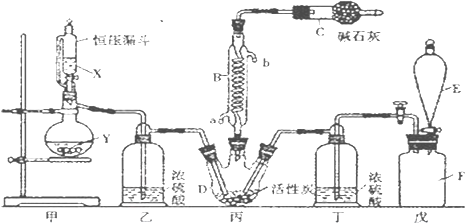
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2、NH3、SO3 | B. | CO2、CH4、C2H5OH | C. | NO、CaO、Ne | D. | P4、CS2、Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,1 mol任何物质的体积约为22.4 L | |
| B. | 1 mol气体的体积约为22.4 L | |
| C. | 1 mol氖气和1 mol氧气体积相同 | |
| D. | 在标准状况下,1 mol氖气和氯气混合气体(任意体积比)的体积约为22.4 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com