


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
A、 |
B、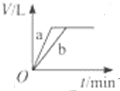 |
C、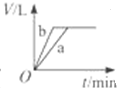 |
D、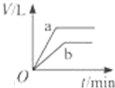 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应后溶液呈碱性,且溶液中OH-的物质的量为1mol |
| B、反应后,铝元素的存在形式有Al(OH)3和AlO2-,且物质的量分别为1mol、0.5mol |
| C、反应后溶液中有K2SO4和KAlO2两种溶质 |
| D、反应中生产沉淀Al(OH)3和BaSO4的物质的量分别为2mol、3.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去乙酸乙酯中少量乙酸:加入乙醇和浓硫酸,使乙酸转化为乙酸乙酯 |
| B、除去氯气中的水蒸气:将气体通过装有浓硫酸的洗气瓶 |
| C、海水淡化:将海水进行蒸馏 |
| D、提取溶解在水中的少量碘:加入CCl4振荡、静置、分层后取出有机层再分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向量热计中加入盐酸,搅拌后的温度为初始温度 |
| B、实验中可使酸或碱略过量 |
| C、向量热计中加碱液时,碱液的温度应与酸的温度相同 |
| D、可以用氢氧化钾代替氢氧化钠,浓硫酸代替盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
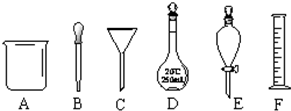
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、①④⑥ |
| C、②③⑤ | D、①②③④⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com