
| ||
| ||


 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
| A、200mL 2mol?L-1MgCl2溶液 |
| B、500mL 2.5mol?L-1NaCl溶液 |
| C、300mL 5mol?L-1CaCl2溶液 |
| D、250mL 1mol?L-1AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、合成染发剂 |
| B、无机染发剂 |
| C、植物染发剂 |
| D、以上三类染发剂均有 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H218O中投入Na2O2固体:2H218O+2O22-=4OH-+18O2↑ |
| B、用双氧水和稀硫酸处理铜板:Cu+H2O2+2H+=Cu2++2H2O |
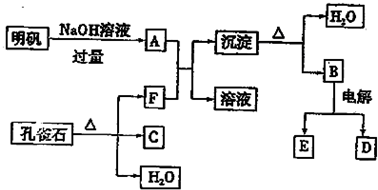
| C、明矾溶液中加入过量的氢氧化钡溶液:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| D、向NaAlO2溶液中通入过量CO2:2 AlO2-+CO2+3H2O=2Al (OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.0L 1.0mo1?L-1的NaAlO2水溶液中含有的氧原子数为2NA |
| B、1molNa2O2和Na2O的混合物中,含阴阳离子总数为3NA |
| C、1molNa被完全氧化生成Na2O2,失去个2NA电子 |
| D、Na2O2与足量H2O反应,共生成2.24LO2,转移电子的数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
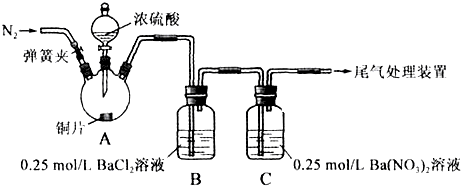
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2, 停止加热,一段时间后关闭 | |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
| 甲 | 少量白色沉淀 |
| 乙 | 大量白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 清洁剂名称 | 洁厕灵 | 活氧彩漂 | 漂白精 |
| 功能 | 有效清除污垢,除异味 | 漂洗衣物,使色彩更鲜艳 | 快速漂除衣物污渍 |
| 有效成分 | HCl | H2O2 | NaClO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com