

| A、Z元素的原子半径可能比Y元素的小 |
| B、W的原子序数可能是Y的原子序数的2倍 |
| C、W的气态氢化物的稳定性一定比Y的强 |
| D、Z的化学活泼性一定比X强 |


科目:高中化学 来源: 题型:
| 1 |
| 16 |
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O2 |
| B、CO |
| C、CO2 |
| D、CO和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室制取乙烯常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫.有人设计下列实验以确证上述混合气体中含有乙烯和二氧化硫.
实验室制取乙烯常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫.有人设计下列实验以确证上述混合气体中含有乙烯和二氧化硫.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
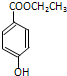 ).
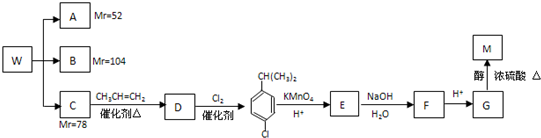
).
查看答案和解析>>
科目:高中化学 来源: 题型:
 反应的H2或溴水中Br2的最大量分别是( )
反应的H2或溴水中Br2的最大量分别是( )| A、11mol,9mol |
| B、9 mol,6mol |
| C、6mol,5 mol |
| D、l3 mol,9mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 稀硫酸 |
| △ |
| 一定条件 |
| 试剂X |
| NaOH溶液 |
| △ |
| [O] |
| H2O |
| [O] |
| [O] |
| KMnO4 |
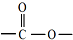 ,且无环状结构的同分异构体有
,且无环状结构的同分异构体有查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com