
以下是某溶液中含有的浓度较大的离子的检验结论,明显错误的是( )
A.Na![]() 、H
、H![]() 、Cl
、Cl![]() 、HCO
、HCO![]()
B.Ca![]() 、Mg
、Mg![]() 、Cl
、Cl![]() 、Br
、Br![]()
C.Na![]() 、OH
、OH![]() 、S
、S![]() 、Cl
、Cl![]()
D.K![]() 、SO
、SO![]() 、NH
、NH![]() 、Cl
、Cl![]()
 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
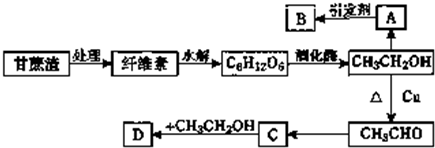
| 引发剂 |
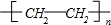
| 引发剂 |
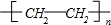
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
查看答案和解析>>
科目:高中化学 来源:2012届山东省威海市高三第一次模拟考试化学试卷 题型:实验题
为研究某铁质材料与浓硫酸反应生成气体的成分,某学习小组进行了以下探究活动:
(1)称取铁钉5.6g放入20mL足量浓硫酸中,加热,理论上收集到气体SO2 L(标况)。将所得气体全部通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体23.3g。由此推知实际生成气体SO2的体积为 L(标况)。
(2)分析上述实验中SO2体积的结果,有同学认为所得气体中除含有 SO2外,还可能含有H2和Q气体。为此设计了下
SO2外,还可能含有H2和Q气体。为此设计了下 列探究实验装置(图中夹持仪器省略)。
列探究实验装置(图中夹持仪器省略)。
①装置A中试剂的作用是 
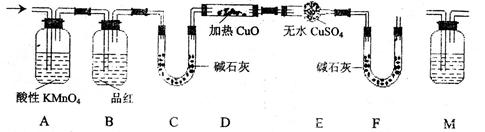
②认为气体中还含有的Q气体是
③为确认Q的存在,需在装置中添加M于 ,
a.A之前 b.AB之间 c.BC之间 d.CD之间
M中的试剂是
④如果气体中含有H2,预计实验现象应是 
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省威海市高三第一次模拟考试化学试卷 题型:实验题
为研究某铁质材料与浓硫酸反应生成气体的成分,某学习小组进行了以下探究活动:
(1)称取铁钉5.6g放入20mL足量浓硫酸中,加热,理论上收集到气体SO2 L(标况)。将所得气体全部通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体23.3g。由此推知实际生成气体SO2的体积为 L(标况)。
(2)分析上述实验中SO2体积的结果,有同学认为所得气体中除含有SO2外,还可能含有H2和Q气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
①装置A中试剂的作用是
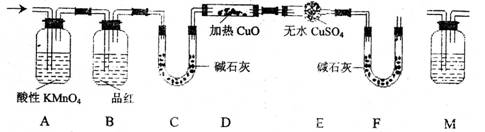
②认为气体中还含有的Q气体是
③为确认Q的存在,需在装置中添加M于 ,
a.A之前 b.AB之间 c.BC之间 d.CD之间
M中的试剂是
④如果气体中含有H2,预计实验现象应是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com