

���� ��ϡ���ᴦ����ʯʱ������ͭ��������ͭ����������������֮������Ӧ����ʯ��SiO2������Ӧ�����˵õ���Һ�м����л���ȡ����Һ�õ��л����ˮ���ˮ����е���Ҫ��������������ѭ��ʹ�ã��л����м��뷴��ȡ����Һ�õ�ˮ��2����ɫ˵����ȡ��ͭ���ӣ���Ҫ�ɷ�������ͭ�������ͭ��Һ�õ���ͭ��ϡ���ᣬ�л���ȡ����ϡ����ѭ��ʹ�ã�
��1���������Ϣ֪������ͭ��������Һ�в��ȶ����ɷ�������������ԭ��Ӧ����ͭ������ͭ���Ŵ�ʪ����ͭ����Ҫ��Ӧ�����û�ͭ��
��2��ˮ��2����Ҫ�ɷ�������ͭ���������ͭ��Һʱ��������ˮ�������OH-�ŵ������������������Cu2+�ŵ�����ͭ��
��3��ˮ��1�е���Ҫ������������������ϡ�����ܽ�ʱ���ɵ�ͭ����������Ӧ������������������ͭ�����������ѭ����ȡ��������������Ũ�ȹ����뽫���������ʸþ�������ˮ���������������������е����������ױ������е������������ʷ����ڿ����е���Һ��ɫ����
��4�����ʯ�к��д��������ʣ���ֱ�����û�ԭ�����õ�ͭ�к��д������������ܷ�Ӧ�Ķ�����������ʣ�������ͭʵ��Ӧ�ü�ֵ��С�������������쵼�����Ӳ�Ʒ�ȣ�
��� �⣺��������ͼ����ϡ���ᴦ����ʯʱ������ͭ��������ͭ����������������֮������Ӧ����ʯ��SiO2������Ӧ�����˵õ���Һ�м����л���ȡ����Һ�õ��л����ˮ���ˮ����е���Ҫ��������������ѭ��ʹ�ã��л����м��뷴��ȡ����Һ�õ�ˮ��2����ɫ˵����ȡ��ͭ���ӣ���Ҫ�ɷ�������ͭ�������ͭ��Һ�õ���ͭ��ϡ���ᣬ�л���ȡ����ϡ����ѭ��ʹ�ã�
��1����ϡ���ᴦ����ʯʱ������ͭ��������ͭ����������������֮������Ӧ���������Ϣ֪������ͭ��������Һ�в��ȶ����ɷ�������������ԭ��Ӧ����ͭ������ͭ����������ͭ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ��Cu2O+H2SO4=CuSO4+Cu+H2O����Ӧ�����ӷ���ʽΪ��Cu2O+2H+=Cu2++Cu+H2O���Ŵ�ʪ����ͭ����Ҫ��Ӧ�����ӷ���ʽΪ��Fe+Cu2+=Fe2++Cu��
�ʴ�Ϊ��Cu2O+2H+=Cu2++Cu+H2O��Fe+Cu2+=Fe2++Cu��
��2��ˮ��2����Ҫ�ɷ�������ͭ���������ͭ��Һʱ��������ˮ�������OH-�ŵ�����������缫��ӦΪ��4OH--4e-=O2��+2H2O����������Cu2+�ŵ�����ͭ���缫��ӦΪ��Cu2++2e-=Cu��
�ʴ�Ϊ��4OH--4e-=O2��+2H2O��Cu2++2e-=Cu��
��3��ˮ��1�е���Ҫ������������������ϡ�����ܽ�ʱ���ɵ�ͭ����������Ӧ������������������ͭ�����������ѭ����ȡ��������������Ũ�ȹ����뽫���������ʸþ�������ˮ��������������ѧʽΪFeSO4•7H2O�����������е����������ױ������е������������ʷ����ڿ����е���Һ��ɫ����������Ӧ�����ӷ���ʽ��4Fe2++O2+4H+=4Fe3++2H2O��
�ʴ�Ϊ��FeSO4•7H2O��4Fe2++O2+4H+=4Fe3++2H2O��
��4�����ʯ�к��д��������ʣ���ֱ�����û�ԭ�����õ�ͭ�к��д������������ܷ�Ӧ�Ķ�����������ʣ�������ͭʵ��Ӧ�ü�ֵ��С�������������쵼�����Ӳ�Ʒ�ȣ�
�ʴ�Ϊ�����д������ʶ�Ӱ��ͭ�ĵ����ԣ�
���� ���⿼����ͭ���仯��������ʣ��������ǿ���Ƚϡ����ʵķ�����ᴿ��������ԭ��Ӧ�ļ��㣬�漰�ķ���ʽ�Ƚ϶࣬�Ѷ��еȣ���Ҫ�����������ȡ���е���Ϣ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.08mol/L | B�� | 0.08mol/��L•s�� | C�� | 0.04mol/��L•min�� | D�� | 0.04 mol/��L•s�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | þ�����ܺ���ˮ�������ҵķ�Ӧ | B�� | ����Mg��OH��2��Al��OH��3 | ||
| C�� | �ȶ���SiH4��HCl | D�� | ������Na��Mg |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������ | ����Һ�������mL�� | ����0.4000mol•L-1����������mL�� | |
| �ζ�ǰ��mL�� | �ζ���mL�� | ||
| 1 | 20.00 | 2.10 | 22.00 |
| 2 | 20.00 | 0.90 | 21.00 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ijУ��ѧ��ȤС��̽��SO2��FeCl3��Һ�ķ�Ӧ������װ������ͼ��ʾ���г���������ȥ����
ijУ��ѧ��ȤС��̽��SO2��FeCl3��Һ�ķ�Ӧ������װ������ͼ��ʾ���г���������ȥ����| ����� | ��5mL��1mol•LFeCl3��Һ��ͨ��SO2���壬��Һ������Ϊ����ɫ�����ڽ϶�ʱ������Һ��ɫ��Ϊdz��ɫ�� |
| ����� | ��5mL�������Ƶ�1mol•L-1��FeCl3��Һ����Ũ�����ữ����ͨ��SO2���壬��Һ������Ϊ����ɫ����ʱ���ڷ�����Һ��ɫ���dz��ɫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
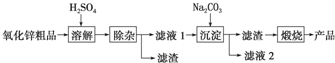
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com