
| ѡ�� | ʵ����� | ʵ������ | ʵ����� |
| A | NaHCO3��Һ��NaAlO2��Һ��� | ���ɰ�ɫ���� | ���H+�������� CO32-��AlO2- |
| B | �����£���ͬ����Ƭ�ֱ�Ͷ��������ϡ��Ũ������ | Ũ��������Ƭ���ܽ��� | ��Ӧ��Ũ��Խ��Ӧ����Խ�� |
| C | ��2mL 2%��CuSO4��Һ�м���0.5mL 1%��NaOH��Һ������뼸���л��Լ�X����Һ������ | δ����ש��ɫ���� | �л��Լ�X�в���ȩ�� |
| D | 2mL 0.1mol/L��NaOH��Һ�еμ�2��0.1mol/L��MgCl2��Һ���ٵμ�2��0.1mol/L��FeCl3��Һ | ��ɫ����ת��Ϊ���ɫ���� | �ܽ�ȣ� Mg��OH��2��Fe��OH��3 |
| A�� | A | B�� | B | C�� | C | D�� | D |
���� A��NaAlO2��H+��Ӧ���ɳ������ٽ�HCO3-�ĵ��룻
B��Ũ�������������ۻ���Ӧ��
C��Ӧ�ڼ��������·���������ԭ��Ӧ��
D���������ܵ���ʵ�ת���жϣ�
��� �⣺A��NaAlO2��H+��Ӧ���ɳ������ٽ�HCO3-�ĵ��룬���֤�����H+��������CO32-��AlO2-����A��ȷ��
B��Ũ�������������ۻ���Ӧ���������ڱȽϷ�Ӧ���ʣ���B����
C��Ӧ�ڼ��������·���������ԭ��Ӧ����ʵ��������٣���C����
D����2mL 0.1mol•L-1 NaOH��Һ�еμ�2��0.1mol•L-1 MgCl2��Һ���������ƹ������ٵμ�2��0.1mol•L-1 FeCl3��Һ�����ֺ��ɫ������������������ת������D����
��ѡA��
���� ���⿼���Ϊ�ۺϣ��漰���ԱȽϣ�����ת���Լ�Ԫ�ػ�����֪ʶ��������ѧ���ķ���������ʵ�������Ŀ��飬Ϊ�߿��������ͣ��Ѷȴ�ע�����ʵ�������ԭ����ʵ�鷽����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
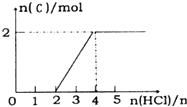
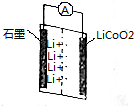 ij����Ӷ��ε��װ����ͼ��ʾ����ŵ�ʱ���ܷ�ӦΪLi1-xCoO2+LixC6�T6C+LiCoO2������˵����ȷ���ǣ�������
ij����Ӷ��ε��װ����ͼ��ʾ����ŵ�ʱ���ܷ�ӦΪLi1-xCoO2+LixC6�T6C+LiCoO2������˵����ȷ���ǣ�������| A�� | ʯīΪ���� | |
| B�� | ���ʱ�������������� | |
| C�� | ���ʱ��������ӦʽΪxLi-xe-�TxLi+ | |
| D�� | �ŵ�ʱ��������ӦΪxLi+Li1-xCoO2+xe-�TLiCoO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ±��Ԫ���ǵ��͵ķǽ���Ԫ�أ�±�ص��ʼ��仯�����������������ж�����Ҫ����;��
±��Ԫ���ǵ��͵ķǽ���Ԫ�أ�±�ص��ʼ��仯�����������������ж�����Ҫ����;�� ��
�� ��
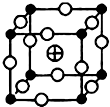
�� �ֱ����һ�����ӣ��������߳�Ϊanm��1nm=10-9m�����þ���Ļ�ѧʽΪKMgF3���þ�����ܶ�Ϊ$\frac{0.1993}{{a}^{3}}$g•cm-3��
�ֱ����һ�����ӣ��������߳�Ϊanm��1nm=10-9m�����þ���Ļ�ѧʽΪKMgF3���þ�����ܶ�Ϊ$\frac{0.1993}{{a}^{3}}$g•cm-3���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
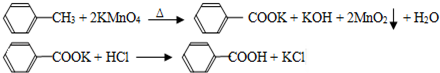
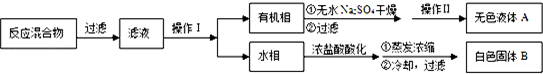
| ��� | ʵ�鷽�� | ʵ������ | ���� |
| �� | ����ɫ����B����ˮ�У������� �⣬��ȴ������ | �õ���ɫ�������ɫ��Һ | ----------------- |
| �� | ȡ������Һ���Թ��У����������������ữ��AgNO3��Һ | ���ɰ�ɫ���� | ��Һ��Cl- |
| �� | �����ɫ���壬����ʹ���ڻ��������۵� | �۵�Ϊ122.4�� | ��ɫ�����DZ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Һ������ʱҪ���մ������ȣ������������ | |
| B�� | ѹ��ȼú���ϸ�س���������ҵ��������������Ч��ʩ | |
| C�� | �ֻ����������̼��ά��Ĥ��һ�����͵����ǽ������� | |
| D�� | ������Ͻ��ǵ�������ҵ����ͥ�㷺ʹ�õIJ��ϣ�����Ϊ�������������ĸ�ʴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
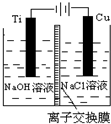 ����Cu2O���ھ��������Ĵ����ܶ��ܵ���ע���������ӽ���Ĥ�����������Һ��OH-��Ũ���Ʊ�����Cu2O��װ����ͼ��ʾ���ܷ�ӦΪ2Cu+H2O$\frac{\underline{\;���\;}}{\;}$Cu2O+H2��������˵������ȷ���ǣ�������
����Cu2O���ھ��������Ĵ����ܶ��ܵ���ע���������ӽ���Ĥ�����������Һ��OH-��Ũ���Ʊ�����Cu2O��װ����ͼ��ʾ���ܷ�ӦΪ2Cu+H2O$\frac{\underline{\;���\;}}{\;}$Cu2O+H2��������˵������ȷ���ǣ�������| A�� | �ѣ�Ti���缫���淢��������Ӧ | |
| B�� | ����������Һ��pH��С | |
| C�� | ���ӽ���Ĥ�˲��������ӽ���Ĥ | |
| D�� | ���������ܷ�Ӧʽ�ǣ�2Cu+2OH--2e-�TCu2O+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 A��B��C��D��E �ֱ������ѧ��ѧ�еij������ʣ��������ĿҪ��ش��������⣺
A��B��C��D��E �ֱ������ѧ��ѧ�еij������ʣ��������ĿҪ��ش��������⣺ ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
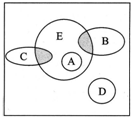 ��ͼ�����������ʾ���еĻ�ѧ��Ӧ����Ȧ�������ʾ������ԭ��Ӧ����Ȧ�������ʾ��������ԭ��Ӧ������A��D�ֱ��ʾ4�ֻ�����Ӧ���ͣ�
��ͼ�����������ʾ���еĻ�ѧ��Ӧ����Ȧ�������ʾ������ԭ��Ӧ����Ȧ�������ʾ��������ԭ��Ӧ������A��D�ֱ��ʾ4�ֻ�����Ӧ���ͣ��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com