
| A. | 常温常压下,22.4 L乙烯中C-H键数为4NA | |
| B. | 1 mol羟基中电子数为10NA | |
| C. | 在反应KIO3+6HI═KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA | |
| D. | 常温下,1 L 0.1 mol•L-1 的NH4NO3溶液中氮原子数为0.2NA |
分析 A.标准状况下气体摩尔体积为22.4L/mol;
B.羟基是中性取代基,1个羟基中含电子数9个电子;
C.KIO3+6HI═KI+3I2+3H2O中碘元素化合价+5价变化为0价,-1价变化为0价,电子转移总数为5e-;
D.依据溶液中氮元素守恒分析计算;
解答 解:A.标准状况下气体摩尔体积为22.4L/mol,常温常压下,22.4 L乙烯物质的量不是1mol,故A错误;
B.羟基是中性取代基,1个羟基中含电子数9个电子,1 mol羟基中电子数为9NA,故B错误;
C.KIO3+6HI═KI+3I2+3H2O中碘元素化合价+5价变化为0价,-1价变化为0价,电子转移总数为5e-,每生成3 mol I2转移的电子数为5NA,故C错误;
D.依据溶液中氮元素守恒分析计算,常温下,1 L 0.1 mol•L-1 的NH4NO3溶液中溶质物质的量=1L×0.1mol/L=0.1mol,氮原子数为0.2NA,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件应用、基团结构、氧化还原反应电子转移的计算等,掌握基础是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液 | B. | NaOH溶液 | C. | KSCN溶液 | D. | 氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数为94、中子数为144的钚(Pu)原子:14494Pu | |
| B. | H2O2的电子式: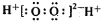 | |
| C. | S2-离子结构示意图: | |
| D. |  的名称2-甲基-4-丁醇 的名称2-甲基-4-丁醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
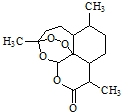
| A. | 青蒿素分子式为C15H20O5 | |
| B. | 可用蒸馏水提取植物中的青蒿素 | |
| C. | 青蒿素在碱性条件下易发生水解反应 | |
| D. | 青蒿素遇湿润的淀粉碘化钾试纸立刻显蓝色,是因为分子结构中含有酯基 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 理论上说,任何能自发进行的氧化还原反应都可设计成原电池 | |
| B. | 某原电池反应为Cu+2AgNO3═Cu(NO3)2+2Ag,装置中的盐桥内可以是含琼脂的KCl饱和溶液 | |
| C. | 因为铁的活泼性强于铜,所以将铁、铜用导线连接后放入浓硝酸中组成原电池,必是铁做负极、铜做正极 | |
| D. | CaO+H2O═Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯(SO2、H2O):碱石灰,洗气 | B. | 乙烷(乙烯):酸性 KMnO4,洗气 | ||
| C. | 炭粉(MnO2):热的浓盐酸,过滤 | D. | Cl2(HCl):饱和食盐水,洗气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com