
| 编号 | 实践操作 | 实验主要现象 | 离子方程式 |
| ① | 加入过量铁粉 | | |
| ② | 加入少量Na2O2粉末 | | |
| ③ | 加入少量AgNO3溶液 | | |
| 编号 | 实验操作 | 实验主要现象 | 离子方程式 |
| ① | 加入过量铁粉 | 铁粉部分溶解,溶液由棕黄色变浅绿色 | 2Fe3++Fe=3Fe2+ |
| ② | 加入少量 Na2O2粉末 | 生成红褐色沉淀并放出无色无味气体 | 2Na2O2+2H2O=4Na++4OH-+O2↑ Fe3++3OH-=Fe(OH)3↓ |
| ③ | 加入少量 AgNO3溶液 | 生成白色沉淀 | Ag++Cl-=AgCl↓ |


科目:高中化学 来源:不详 题型:填空题
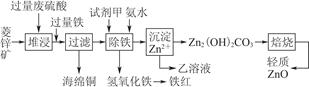
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.3 | 9.7 |
| Fe3+ | 1.5 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.赤铁矿的主要成分是Fe3O4 |
| B.钢铁在湿空气中生锈,生成Fe2O3和H2 |
| C.除去FeCl2溶液中的FeCl3杂质可以向溶液中加铁粉,然后过滤 |
| D.Fe3+与KSCN反应产生红色沉淀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3︰1 | B.1︰2 | C.2︰1 | D.1∶1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 探究内容 | 实验方案 | 实验现象 |
| 探究Fe2+具有还原性 | 取少量0.1 mol·L-1 FeCl2溶液,加入足量__________后,再往溶液中加入少量__________ | 溶液变成血红色 |
| 探究Fe2+具有氧化性 | 取少量0.1 mol·L-1 FeCl2溶 液,加入_________充分 反应 | 溶液由浅绿色变无色 所发生反应离子方程式为________________ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

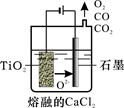
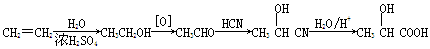
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入粉末质量/g | 13.68 | 27.36 | 34.20 |
| 生成气体的体积(标准状况)/L | 2.912 | 5.824 | 6.720 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
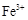 和
和 浓度相等。则已反应的
浓度相等。则已反应的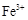 和未反应的
和未反应的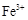 的物质的量之比是
的物质的量之比是| A.2︰3 | B.3︰2 | C.1︰2 | D.1︰1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.混合物里3种物质反应时消耗盐酸的物质的量浓度之比为1︰1︰3 |
| B.反应后所得溶液中的Fe2+离子与Cl-离子的物质的量浓度之比为2︰1 |
| C.混合物里,FeO的物质的量无法确定,但Fe比Fe2O3的物质的量多 |
| D.混合物里,Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com