
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得浊液中逐渐加入1.00mol/LHCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示。
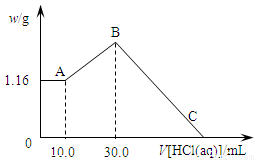
(1)A点的沉淀物的化学式为 。
(2)写出A点至B点发生反应的离子方程式: 。
(3)原混合物中NaOH的质量是 g,C点(此时沉淀恰好完全溶解)HCl溶液的体积为 mL。
(1)Mg(OH)2 (2)AlO2-+H++H2O=Al(OH)3↓ (3)5.20 130.0
【解析】
试题分析:(1)向所得浊液中,逐滴加入1.00mol/L盐酸,由加入盐酸的体积和生成沉淀的质量关系图分析:①0~10ml,随盐酸的体积增加,生成沉淀的质量不变,说明氢氧化钠过量,加入的盐酸与氢氧化铝先反应,方程式为NaOH+HCl=NaCl+H2O。因此A点沉淀是Mg(OH)2,其质量是1.16g,物质的量n=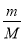 =
=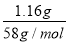 =0.02mol。则根据原子守恒可知原混合物中氯化镁的物质的量=0.02mol。
=0.02mol。则根据原子守恒可知原混合物中氯化镁的物质的量=0.02mol。
(2)NaOH、AlCl3、MgCl2组成的混合物,溶于足量水发生反应是:MgCl2+2NaOH=Mg(OH)2↓+2NaCl、AlCl3+4NaOH=NaAlO2+3NaCl+2H2O。NaOH过量,溶液是NaCl、NaAlO2和NaOH的混合液,则A~B阶段发生反应是:NaAlO2+HCl+H2O=Al(OH)3↓+NaCl,离子方程式是:H2O+AlO2-+H+=Al(OH)3↓。
(3)A~B阶段消耗盐酸的物质的量=(0.03L-0.01L)×1.0mol/L=0.02mol,则根据方程式NaAlO2+HCl+H2O=Al(OH)3↓+NaCl可知生成氢氧化铝的物质的量=0.02mol。所以根据原子守恒可知原混合物中氯化铝的物质的量是0.02mol。B点沉淀达到最大值,此时的沉淀是氢氧化镁和氢氧化铝的混合物。而溶液则恰好是氯化钠溶液。根据氯离子守恒可知氯化钠的物质的量=0.03L×1.00mol/L+0.02mol×2+0.02mol×3=0.13mol。所以根据钠离子守恒可知,氢氧化钠的物质的量也是0.13mol,因此氢氧化钠的质量m=n· M=40g/mol×0.13mol=5.2g。B~C阶段加入的盐酸开始溶解氢氧化铝和氢氧化镁,此时反应的方程式为Mg(OH)2+2HCl=MgCl2+2H2O;Al(OH)3+3HCl=AlCl3+3H2O。根据氢氧化镁和氢氧化铝均是0.02mol可知,该阶段消耗盐酸的物质的量是0.02mol×2+0.02mol×3=0.10mol,其体积是0.10mol÷1mol/L=0.1L=100ml,所以C点(此时沉淀恰好完全溶解)HCl溶液的体积为30ml+100ml=130ml。
考点:考查镁、铝合金与氢氧化钠溶液以及元素反应的有关计算与判断、图像分析与应用


科目:高中化学 来源:2016届广东省梅州市高一上学期质检化学试卷(解析版) 题型:选择题
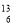 C-NMR(核磁共振)可以用于含碳化合物的结构分析,有关
C-NMR(核磁共振)可以用于含碳化合物的结构分析,有关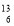 C的说法正确的是( )
C的说法正确的是( )
A、质子数为6 B、电子数为13
C、中子数为6 D、质量数为6
查看答案和解析>>
科目:高中化学 来源:2016届广东省东莞市高一上学期期末考试化学试卷(A)(解析版) 题型:填空题
向10mLNa2CO3和Na2SO4的混合溶液中加入足量的氯化钡溶液,生成沉淀的质量为6.27g,向所得沉淀中加入足量稀盐酸,沉淀质量减少到2.33g,并放出气体,试计算:
(1)原混合物中Na2SO4的物质的量浓度;
(2)在标准状况下产生气体的体积。
查看答案和解析>>
科目:高中化学 来源:2016届广东省东莞市高一上学期期末考试化学试卷(A)(解析版) 题型:选择题
科学家发现,食用虾类等水生甲壳类动物的同时服用维生素C容易中毒,这是因为对人体无害的+5价砷类物质在维生素C的作用下,能够转化为有毒的+3价砷类化合物。下列说法中不正确的是
A.维生素C具有还原性
B.上述过程中砷元素发生还原反应
C.上述过程中+5价砷类物质作氧化剂
D.1 mol+5价砷完全转化为+3价砷,共失去2 mol电子
查看答案和解析>>
科目:高中化学 来源:2016届广东省东莞市高一上学期期末考试化学试卷(A)(解析版) 题型:选择题
PM 2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物。2012年2月,国务院同意发布新修订的《环境空气质量标准》增加了PM 2.5监测指标。下列情况不会增加空气中PM 2.5的是
A.露天焚烧秸秆 B.直接用煤作燃料
C.汽车排放尾气 D.利用太阳能发电
查看答案和解析>>
科目:高中化学 来源:2016届山西省朔州市高一上学期第四次月考化学试卷(解析版) 题型:选择题
下列说法错误的是
A.仅用KSCN可以检验Fe2+ B.可以用NaOH溶液检验Fe3+
C.通过化合反应可以得到Fe(OH)3 D.通过化合反应可以得到FeCl2
查看答案和解析>>
科目:高中化学 来源:2016届山西省朔州市高一上学期第四次月考化学试卷(解析版) 题型:选择题
硫酸亚铁溶液含有杂质硫酸铜和硫酸铁,为除去杂质,提纯硫酸亚铁,应该加入下列哪种物质
A.锌粉 B.镁粉 C.铁粉 D.铝粉
查看答案和解析>>
科目:高中化学 来源:2016届山东省烟台市高一上学期期末统考化学试卷(解析版) 题型:填空题
工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下:
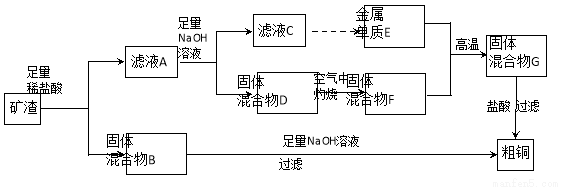
已知:Cu2O+2H+═Cu+Cu2++H2O
(1)固体混合物B与氢氧化钠溶液反应的化学方程式为 。
(2)滤液A中铁元素的存在形式只能为Fe2+,理由是
。涉及的离子方程式为 、
(不必书写Cu2O与盐酸的反应)。检验滤液A中Fe2+的试剂为 (填试剂名称)。
(3)将滤液C中的铝元素以沉淀形式析出,可选用的最佳试剂为 __ (填序号)。
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
金属E与固体F某一成分发生的反应可用于焊接钢轨,该反应的化学方程为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com