

分析 FeCl3与铜箔反应后的溶液中含有CuCl2、FeCl2,在混合液中加入过量铁粉,反应生成Fe2+、Cu,滤渣中含有Fe和Cu,除去其中的Fe选用盐酸,向氯化亚铁溶液中通入氯气生成FeCl3,可重复使用,以此解答该题.
解答 解:FeCl3与铜箔反应后的溶液中含有CuCl2、FeCl2,在混合液中加入过量铁粉,反应生成Fe2+、Cu,滤渣中含有Fe和Cu,除去其中的Fe选用盐酸,向氯化亚铁溶液中通入氯气生成FeCl3,
(1)由以上分析可知B为盐酸,氯化铁与铜反应生成氯化亚铁与氯化铁,反应方程式为:2Fe3++Cu═2Fe2++Cu2+,故答案为:HCl;2Fe3++Cu═2Fe2++Cu2+;
(2)反应③的离子方程式为2Fe2++C12=2Fe3++2C1-,故答案为:2Fe2++C12=2Fe3++2C1-;
(3)反应Fe+Cu2+=Fe2++Cu中,铁可置换出铜,可说明铁的金属活动性比铜强,在步骤②中发生该反应,用该反应设计一个原电池,可用铁为负极,碳棒为正极,硫酸铜或氯化铜溶液作电解质溶液,如图 ,
,
故答案为:Fe+Cu2+=Fe2++Cu; ;
;
(4)流程中FeCl3可循环使用,为步骤③,故答案为:③.
点评 本题考查化学工艺流程、根据方程的计算、元素化合物性质等,掌握元素化合物的性质、混合物的分离、提纯方法是解决本题的关键,题目难度中等.


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠的电子式: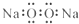 | |
| B. | 硫离子的结构示意图: | |
| C. | NH4Cl的电子式: | |
| D. | 质子数为35、中子数为45的溴原子:${\;}_{35}^{80}$Br |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 节能减排与我们的生活息息相关,参与节能减排是每一位公民应尽的义务.下列举措不符合这一要求的是( )
节能减排与我们的生活息息相关,参与节能减排是每一位公民应尽的义务.下列举措不符合这一要求的是( )| A. | 倡导开私家车的人乘公交车上下班 | |
| B. | 用节能灯代替白炽灯 | |
| C. | 政府鼓励科研和生产部门开发、利用太阳能 | |
| D. | 加快开发石油以缓解能源紧张问题 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “类钫”属过渡元素,具有放射性 | B. | “类钫”可与水剧烈反应 | ||
| C. | “类钫”单质的密度小于1g/cm3 | D. | “类钫”单质有较高熔点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②③④ | C. | ①②④ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子有得失 | B. | 共用电子对有偏移 | ||
| C. | 电子既有得失又有偏移 | D. | 金属元素的存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
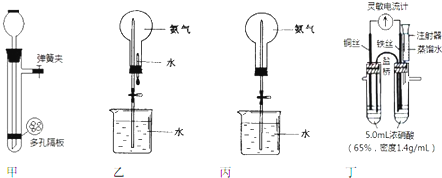
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com