
| A. | 1 mol氧为32 g | |
| B. | 标准状况下,1 mol H2和O2的混合气体的体积约为22.4 L | |
| C. | CO2的摩尔质量为44 | |
| D. | 2 mol•L-1的BaCl2溶液中含Cl-的个数为2.408×1024 |
分析 A.物质的类别指代不明;
B、标准状况下,1摩尔任何理想气体所占的体积都约为22.4升;
C、摩尔质量的单位是g/mol;
D、根据n=cV计算求解.
解答 解:A.物质的类别指代不明,应指明具体的物质,故A错误;
B、1molH2和O2的混合气体在标准状况下的体积约为22.4L,故B正确;
C、摩尔质量的单位是g/mol,所以CO2的摩尔质量为44g/mol,故C错误;
D、根据n=cV公式,要求物质的量必须知道溶液的体积,所以无法求氯离子的物质的量,故D错误;
故选B.
点评 本题考查了摩尔表示微粒的多少、摩尔质量的单位、物质的量浓度的计算和气体摩尔体积的概念分析和应用条件判断,掌握基础是关键,题目较简单.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
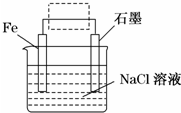 (1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是C.(填字母)
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是C.(填字母)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二者对应的氧化物均为碱性氧化物 | |
| B. | 二者的单质都能与强碱溶液反应生成H2 | |
| C. | 二者的氢氧化物均可以通过化合反应直接制备 | |
| D. | 二者的氯化物均可以通化合反应制备 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| a与b的关系 | 剩余气体的成分 | 剩余气体物质的量 |
| 若a=b | ||
| 若a>b | ||
| 若a<b |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氧和液氢最好在临发射前的一段时间加注 | |
| B. | 氢气可由电解水获得 | |
| C. | 燃烧产物对发射环境没有污染 | |
| D. | 氢是一次能源,可以自己产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com