
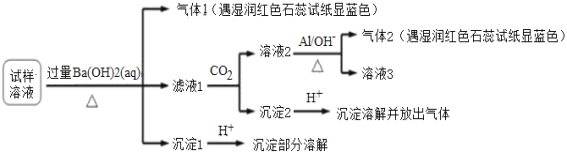
【题目】雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-。某同学收集了该地区的雾霾,经必要的预处理后得试样溶液,设计并完成了如图的实验:
已知:3NO3-+8Al+5OH-+2H2O![]() 3NH3↑+8AlO2-
3NH3↑+8AlO2-
根据以上的实验操作与现象,该同学得出的结论不正确的是()。
A. 试样中肯定存在NH4+、Mg2+、SO42-和NO3-
B. 试样中可能存在Na+、Cl-
C. 试样中一定不含Al3+
D. 该雾霾中可能存在NaNO3、NH4Cl和MgSO4
【答案】C
【解析】
气体1和气体2是氨气,故溶液中一定含有NH4+,生成沉淀1遇酸部分溶解成分是氢氧化镁和硫酸钡,故一定含有Mg2+、SO42-。3NO3-+8Al+5OH-+2H2O![]() 3NH3↑+8AlO2-生成气体2氨气,故溶液2中含有NO3-。沉淀2遇酸沉淀溶解并放出气体,沉淀2是碳酸钡。试样溶液如存在Al3+,加入过量Ba(OH)2溶液,在滤液1中有AlO2-,通入CO2,沉淀2一定会有BaCO3,可能有Al(OH)3,再加酸,现象仍是“沉淀溶解并放出气体”。故试样中可能含Al3+。A. 试样中肯定存在NH4+、Mg2+、SO42-和NO3-,选项A正确;B. 但是根据题目叙述不能确定是否含有Na+、Cl-,它们可能存在,也可能不存在,试样中可能存在,选项B正确;C、通过上述分析可知在试样中可能含有Al3+,选项C不正确;D. 该雾霾中若含有Na+、Cl-,则可能存在NaNO3、NH4Cl和MgSO4,选项D正确;答案选C。
3NH3↑+8AlO2-生成气体2氨气,故溶液2中含有NO3-。沉淀2遇酸沉淀溶解并放出气体,沉淀2是碳酸钡。试样溶液如存在Al3+,加入过量Ba(OH)2溶液,在滤液1中有AlO2-,通入CO2,沉淀2一定会有BaCO3,可能有Al(OH)3,再加酸,现象仍是“沉淀溶解并放出气体”。故试样中可能含Al3+。A. 试样中肯定存在NH4+、Mg2+、SO42-和NO3-,选项A正确;B. 但是根据题目叙述不能确定是否含有Na+、Cl-,它们可能存在,也可能不存在,试样中可能存在,选项B正确;C、通过上述分析可知在试样中可能含有Al3+,选项C不正确;D. 该雾霾中若含有Na+、Cl-,则可能存在NaNO3、NH4Cl和MgSO4,选项D正确;答案选C。


科目:高中化学 来源: 题型:
【题目】下列各溶液中,Na+ 浓度最大的是 ( )
A. 4L 0.5 mol/L NaCl 溶液 B. 1mL 0.3 mol/L Na2SO4 溶液
C. 0.8L 0.4 mol/L NaOH 溶液 D. 3L 0.15 mol/L Na3PO4 溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关溴乙烷的下列叙述中,正确的是( )
A. 在溴乙烷中滴入AgNO3溶液,立即有淡黄色沉淀生成
B. 溴乙烷不溶于水,能溶于大多数有机溶剂
C. 溴乙烷与NaOH的醇溶液反应,可生成乙醇
D. 溴乙烷通常用溴水与乙烷直接反应来制取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸性质是中学化学学习的重点。请回答下列问题:
(1)中学化学中利用物质与浓硫酸共热可制备SO2气体,写出用浓硫酸还可制备不同类别的气体的名称:_____________________写一种)。
(2)某化学兴趣小组为探究铜与浓硫酸的反应以及SO2的性质,用下图所示装置进行有关实验。

①装置B的作用是贮存多余的气体。B中应放置的液体是_______(填序号)
a.饱和Na2SO3溶液 b.酸性 KMnO4溶液
c.浓溴水 d.饱和NaHSO3溶液
②反应完毕后,烧瓶中还有一定量的余酸,使用足量的下列药品不能用来证明反应结束后的烧瓶中的确有余酸的是____(填序号)。
a.Fe粉 b.BaCl2溶液 c.CuO d.Na2CO3溶液
③实验中某学生向A中反应后溶液中通入一种常见气体单质,使铜片全部溶解且仅生成硫酸铜溶液,该反应的化学方程式是_________。
④为验证二氧化硫的还原性,C中盛有氯水,充分反应后,取C中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是___(填“I”、“Ⅱ”或“Ⅲ”);C中发生反应的离子方程式为____________。D中盛有氢氧化钠溶液,当通入二氧化硫至试管D中溶液显中性时,该溶液中c(Na+)=______(用含硫微粒浓度的代数式表示)。
(3)利用FeCl3溶液的氧化性也可以吸收SO2。该反应的离子方程式是_____________。检验FeCl3是否完全被还原的方法为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是与人类生活密切相关的一种重要元素。根据要求回答:
(1)写出N2的电子式_________;将空气中的氮气转化为含氮化合物的过程称为固氮,当今大规模人工固氮的主要方法是(用化学方程式表示)______________________________。
(2)某无色混合气体中可能含有NH3、O2、H2、NO、HCl等气体,将它通过浓H2SO4 后发现气体体积减少,将剩余气体与空气接触后呈红棕色,此混合气中一定不含有_________。
(3)实验室有多种制取氨气的方法,其中加热消石灰与氯化铵的混合固体就是方法之一。
①写出此反应的化学方程式:_____________________________________________。
②氨气可使湿润的红色石蕊试纸变蓝的原因(用相应的方程式说明)_______________。
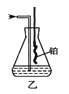
③用乙装置(见图)吸收一段时间氨气后,再通入空气,同时将加热的铂丝插入乙装置的锥形瓶内,锥形瓶中不可能生成的物质是___(选填序号)。
a H2 b NO2 c HNO3 d NH4NO3
写出乙装置中氨催化氧化的化学方程式:__________________________。
(4)已知3Cl2+2NH3==N2 + 6HCl,若NH3过量则还有反应:NH3+ HCl== NH4Cl 。常温常压下,若在一密闭容器中将15mLCl2和40mL NH3充分混合反应后,剩余气体的体积为____mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄可用于酿酒。
(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是_______________________________________。
(2)葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式。
C6H12O6(葡萄糖)![]() 2________+2C2H5OH
2________+2C2H5OH
(3)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备。实验室用下图所示装置制备乙酸乙酯:
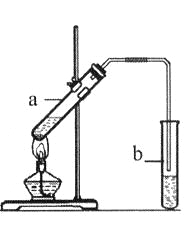
①试管a中生成乙酸乙酯的化学方程式是________________________________。
②试管b中盛放的试剂是饱和_________________溶液。
⑧实验开始时,试管b中的导管不伸入液面下的原因是___________________。
④若分离出试管b中生成的乙酸乙酯,需要用到的仪器是____(填序号)。
a. 漏斗 b. 分液漏斗 c. 长颈漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置进行实验,装置正确且能达到相应实验目的是
A. 析氢腐蚀 B. 证明二氧化氮生成四氧化二氮为放热反应
B. 证明二氧化氮生成四氧化二氮为放热反应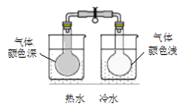 C. 测定溶液pH
C. 测定溶液pH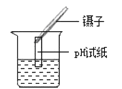 D. 测定盐酸浓度
D. 测定盐酸浓度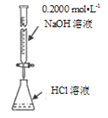
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向浓度均为0.1 molL-1、体积均为100 mL的两种一元酸HX、HY的溶液中,分别加入NaOH固体,lg![]() 随加入NaOH的物质的量的变化情况如图所示。下列叙述正确的是
随加入NaOH的物质的量的变化情况如图所示。下列叙述正确的是

A. HX的酸性弱于HY的
B. a点由水电离出的c(H+)=1×10-12 molL-1
C. c点溶液中:c(Y-)>c(HY)
D. b点时酸碱恰好完全中和
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com