
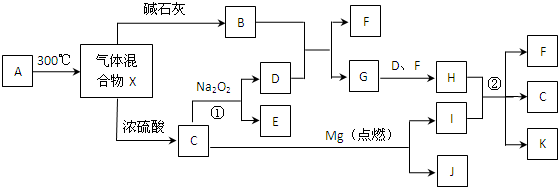
分析 根据题中各物质转化关系,C能与过氧化钠反应且镁可在其中点燃,则C为CO2,B为X经过碱石灰后得的气体,应为碱性或中性气体,能与D反应,则D为O2,B为NH3,图所示转化关系所得B、C的物质的量相等,则A为NH4HCO3,E为Na2CO3,气体混合物X为等物质的量的NH3、CO2、H2O,氨气氧化得一氧化氮,一氧化氮与氧气、水可生成硝酸,二氧化碳与镁可得氧化镁和碳,而碳与浓硝酸反应可得二氧化碳、二氧化氮、水,据此可推断F为H2O,G为NO,H为HNO3,I为C,J为MgO,K为NO2,符合各物质转化关系,据此答题.
解答 解:根据题中各物质转化关系,C能与过氧化钠反应且镁可在其中点燃,则C为CO2,B为X经过碱石灰后得的气体,应为碱性或中性气体,能与D反应,则D为O2,B为NH3,图所示转化关系所得B、C的物质的量相等,则A为NH4HCO3,E为Na2CO3,气体混合物X为等物质的量的NH3、CO2、H2O,氨气氧化得一氧化氮,一氧化氮与氧气、水可生成硝酸,二氧化碳与镁可得氧化镁和碳,而碳与浓硝酸反应可得二氧化碳、二氧化氮、水,据此可推断F为H2O,G为NO,H为HNO3,I为C,J为MgO,K为NO2,符合各物质转化关系,
(1)根据上面的分析可知,A为NH4HCO3,G为NO,
故答案为:NH4HCO3;NO;
(2)反应①的反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,反应②的反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O,
故答案为:2Na2O2+2CO2=2Na2CO3+O2;C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O;
(3)气体混合物X为等物质的量的NH3、CO2、H2O,其平均摩尔质量为$\frac{79}{3}$g/mol,所以同温同压下,气体混合物X对氢气的相对密度是$\frac{79}{3×2}$=13.2,
故答案为:13.2;
(4)把少量NaOH溶液滴入足量NH4HCO3的稀溶液中,其反应离子方程式为OH-+HCO3-=H2O+CO32-,
故答案为:OH-+HCO3-=H2O+CO32-.
点评 本题考查无机物的推断,题目难度中等,根据物质的典型性质,明确物质的种类为解答该题的关键,答题时注意熟练掌握常见元素及其化合物的有关反应,(4)为本题的易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 位于第八周期,第ⅡA族 | |
| B. | 最高价氧化物对应水化物具有强碱性 | |
| C. | 此元素的原子半径较大,熔沸点很高 | |
| D. | 属于人造元素,自然界不存在,并具有放射性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
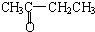 B.
B.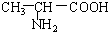 与
与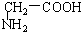
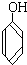 与
与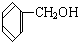 D.CH3CH2C≡CH与CH2=CH-CH=CH2
D.CH3CH2C≡CH与CH2=CH-CH=CH2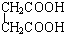 与
与  F.戊烯和环戊烷
F.戊烯和环戊烷查看答案和解析>>
科目:高中化学 来源: 题型:解答题
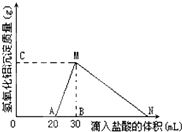 在10mL含有AlO2-离子的溶液中逐滴加入1mol/L的盐酸,所得Al(OH)3沉淀质量和所加盐酸的体积关系如图所示.问:
在10mL含有AlO2-离子的溶液中逐滴加入1mol/L的盐酸,所得Al(OH)3沉淀质量和所加盐酸的体积关系如图所示.问:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
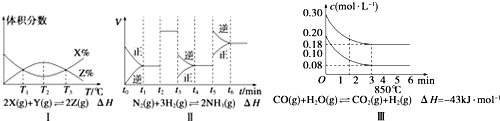
| A. | 由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的△H<0 | |
| B. | 由图Ⅱ知,反应在t6时刻,NH3体积分数最大 | |
| C. | 由图Ⅱ知,t3时采取降低反应体系压强的措施 | |
| D. | 图Ⅲ表示在10 L容器、850℃时的反应,由图知,到4 min时,反应放出51.6 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Cu(OH)2浊液中滴加醋酸:Cu(OH)2+2H+═Cu2++2H2O | |
| B. | NaOH溶液中加入铝片:2Al+2 OHˉ═2AlO2ˉ+3H2↑ | |
| C. | 已知Fe2+可以还原C12、Br2,C12可以氧化Br-生成Br2,在标准状况下,向10mL 0.1moL/LFeBr2溶液中通入22.4mL氯气:2Fe2++2Br-+2C12═2Fe3++Br2+4C1- | |
| D. | NaHCO3溶液与稀硫酸溶液的反应:HCO3-+H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:纯碱>石灰石>小苏打>碳酸 | |
| B. | 除Li外其它碱金属单质均可以保存在煤油中 | |
| C. | 碱金属都是活泼的金属元素,其盐都不发生水解 | |
| D. | 最高氧化物对应水化物碱性LiOH<NaOH<KOH<RbOH<CsOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1>Q2,Q2=2Q3 | B. | Q1=Q2=Q3 | C. | Q1<Q2,Q3=$\frac{{Q}_{1}}{2}$ | D. | 无法比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com