
【题目】钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)向CuSO4溶液中逐滴滴加氨水至过量,过程中会先有沉淀生成,后沉淀逐渐溶解。
①写出沉淀溶解过程的离子方程式___________________。
②Cu2+基态时核外电子排布式为____________________。
③金属铜采取_____堆积。
④NH3分子空间构型为__________________。
(2)制备CrO2Cl2的反应为:K2Cr2O7+3CCl4=2KC1+2CrO2Cl2+3COC12↑。
①上述化学方程式中非金属元素电负性由大到小的顺序是_____________(用元素符号表示)。
②COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为_____,中心原子的杂化方式为____________________。
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相似,其中Ni2+和Fe2+的离子半径分别为6.9×10-2nm和7.8×10-2nm,则熔点:NiO____FeO(填“>”、“<”或“=”)。
(4)Ni和La的合金是目前使用广泛的储氢材料。具有大容量、高寿命、耐低温等特点,在日本和中国己实现了产业化。该合金的晶胞结构如下图所示。

①该晶体的化学式为_______________________。
②已知该晶胞的摩尔质量为Mg/mol,密度为dg·cm-3。设NA为阿伏加德罗常数的值,则该晶胞的体积是_________cm3(用含M、d、NA的代数式表示)。
【答案】 Cu(OH)2+4NH3H2O=[Cu(NH3)4]2++2OH-+4H2O 1s22s22p63s23p63d9或[Ar]3d9 面心立方最密堆积 三角锥形 O>Cl>C 3:1 sp2 > LaNi5 M/NAd
【解析】本题考查物质结构与性质。
解析:(1)①向CuSO4溶液中逐滴滴加氨水时,先生成蓝色的氢氧化铜沉淀,继续滴加氨水,蓝色的氢氧化铜沉淀与氨水反应,生成深蓝色溶液的铜氨络离子,反应的离子方程式为:Cu2++2NH3H2O=Cu(OH)2↓+2NH4+,Cu(OH)2+4NH3H2O=[Cu(NH3)4]2++2OH-+4H2O;②Cu原子核外电子排布为1s22s22p63s23p63d104s1,4s与3d能级各失去1个电子形成Cu2+,则Cu2+基态核外电子排布式为1s22s22p63s23p63d9;③金属Cu采取面心立方堆积;④NH3分子中N原子的价层电子对数为4,孤对电子对数为1,则空间构型为三角锥形。(2)①反应中有O、C、Cl三种非金属元素参与反应,元素的非金属性越强,电负性越大,非金属性强弱顺序为O>Cl>C,由大到小的顺序是O>Cl>C;②由题意可知,COCl2分子中含有1个C、O双键和2个C、Cl单键,单键都是σ键,双键中1个为σ键和1个π键,则COCl2分子中σ键和π键的个数比为3∶1;因分子中含有C、O双键,所以C原子为sp2杂化。(3)Ni0、Fe0的晶体结构类型均与氯化钠的相同,说明二者都是离子晶体,离子晶体的熔点与离子键的强弱有关,离子所带电荷数越多,离子半径越小,离子键越强,熔点越高.由于Ni2+的离子半径小于Fe2+的离子半径,属于熔点是NiO>FeO。(4)①从图中可以看出,La位于平行六面体的顶点,晶胞中La的原子数为8×![]() =1,平行六面体的上、下两个面各有2个Ni原子,四个侧面各有1个Ni原子,体心还有1个Ni原子,晶胞中Ni的原子数为8×
=1,平行六面体的上、下两个面各有2个Ni原子,四个侧面各有1个Ni原子,体心还有1个Ni原子,晶胞中Ni的原子数为8×![]() +1=5,则该晶体的化学式为LaNi5;②晶胞中含有1个LaNi5,晶胞的质量为
+1=5,则该晶体的化学式为LaNi5;②晶胞中含有1个LaNi5,晶胞的质量为![]() ×M, 根据m=dV,晶胞的体积为
×M, 根据m=dV,晶胞的体积为![]() cm3。点晴:本题难点是晶胞结构的分析与与有关计算。使用均摊法计算晶胞微粒个数时,应意晶胞的形状,不同形状的晶胞应先分析任意位置上的一个微粒被几个晶胞所共有,如六棱柱晶胞中顶点、侧棱点、底面棱点和面心点依次被6、3、4、2不晶胞所共有。
cm3。点晴:本题难点是晶胞结构的分析与与有关计算。使用均摊法计算晶胞微粒个数时,应意晶胞的形状,不同形状的晶胞应先分析任意位置上的一个微粒被几个晶胞所共有,如六棱柱晶胞中顶点、侧棱点、底面棱点和面心点依次被6、3、4、2不晶胞所共有。


科目:高中化学 来源: 题型:
【题目】常温下,二氯化二硫(S2Cl2)为橙黄色液体,遇水易水解,工业上用于橡胶的硫化。某学习小组用氯气和硫单质合成S2Cl2的实验装置如图所示,下列说法不正确的是( )
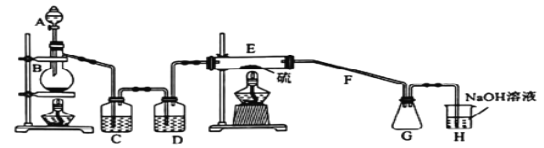
A. 实验时需后点燃E处的酒精灯
B. C、D中所盛试剂为饱和氯化钠溶液、浓硫酸
C. 二氯化二硫(S2Cl2)水解反应产物为S、H2S、HCl
D. G、H之间应加上D装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某混合物A,含有KAl(SO4)2、Al2O3和Cu2(OH)2CO3,在一定条件下可实现下图所示的物质之间的变化:
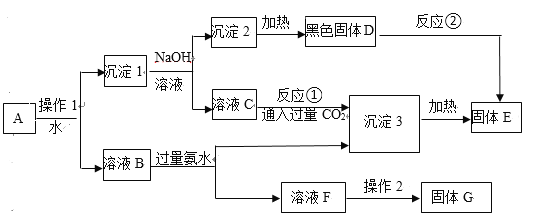
据此判断:
(1)固体G中含有用作化肥的物质,写出其化学式_________。
(2)出土的青铜器上常有铜绿,请写出用稀硫酸除去铜绿的离子方程式_________。
(3)操作1的名称____________; 反应①的离子方程式为____________。
(4)反应②的化学方程式为______________。
II.铝是一种应用广泛的金属,工业上常用冰晶石(Na3AlF6)作助熔剂来冶炼铝。以萤石(CaF2)和纯碱为原料制备冰晶石的流程如下:
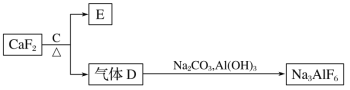
(5)E在医疗上常用作石膏绷带,D的水溶液可用于刻蚀玻璃,C的化学式为_____;并写出由D制备冰晶石的化学方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象或图像信息不能充分说明相应的化学反应是放热反应的是( )
反应装置或图像 | 实验现象或图像信息 | |
A |
| 反应开始后,针筒活塞向右移动 |
B |
| 反应物总能量大于生成物总能量 |
C |
| 反应开始后,甲处液面低于乙处液面 |
D |
| 温度计的水银柱不断上升 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】索氏制碱又称氨碱法,其主要生产流程如左下图:
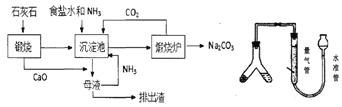
(1)粗盐中常含Ca2+、Mg2+、SO42-等杂质离子,可依次加入NaOH、____、____、盐酸试剂来进行提纯。
(2)用化学方程式表示沉淀池中发生的反应为________________________________。
(3)氨碱法制得的纯碱样品中可能会含有MaCl杂质。现用量气法测定纯碱样品的纯度,(如右上图)如何检查该装置的气密性_________________________________,称取m克样品装入Y型管左侧,量气管中液体应为______________(填字母)。
A.水 B.饱和食盐水 C.饱和碳酸钠溶液 D.饱和碳酸氢钠溶液
(4)若最后测得产生CO2气体的体积为VL(标况下),则样品中纯碱的纯度为_________。若最后读数时,发现水准管液面高于量气管(其他操作都正确),则计算所得纯碱样品的纯度值_____(填“偏大”,“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某同学将等体积的甲烷与氯气混合于一试管中,倒扣在盛饱和食盐水的水槽里,然后置于光亮处。一段时间后的现象正确的是:_____;
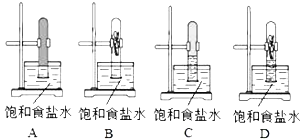
(2)反应后试管中所得有机产物化学式为______________;(有几种写几种)
(3)写出甲烷与氯气反应第一步的化学方程式_________;
(4)在同温同压下,甲烷的同系物A的蒸汽密度是甲烷密度的4.5倍,其分子式__;
(5)A有____种同分异构体;写出其有三个甲基的同分异构体的结构简式___;
(6)A的某同分异构体只有一种一氯代物,请用系统命名法为该同分异构体命名_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】假如你是某化工厂的总工程师,为了加快化学反应速率进而提高经济效益,你应优先考虑的措施是
A.选用适宜的催化剂B.采用高压
C.采用高温D.增大反应物的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,1mol化学键断裂形成气态原子所需要的能量用![]() 表示。结合表中信息判断下列说法不正确的是( )
表示。结合表中信息判断下列说法不正确的是( )
共价键 | H-H | F-F | H-F | H-Cl | H-I |
E(kJ/mol) | 436 | 157 | 568 | 432 | 298 |
A. 432kJ/mol>E(H-Br)>298kJ/mol B. 表中最稳定的共价键是H-F键
C. H2(g)→2H(g) △H=+436kJ/mol D. H2(g)+F2(g)=2HF(g) △H=-25kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验误差分析错误的是
A. 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
B. 滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
C. 用润湿的pH试纸测稀碱溶液的pH,测定值偏小
D. 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com