
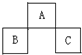
 A、B、C均为周期表中的短周期的元素,它们在周期表的位置如下图.已知B、C两元素在周期表中族数之和是A元素族数的2倍;B、C元素的原子序数之和是A 元素的原子序数的4倍,则A、B、C所在的一组是 ( )
A、B、C均为周期表中的短周期的元素,它们在周期表的位置如下图.已知B、C两元素在周期表中族数之和是A元素族数的2倍;B、C元素的原子序数之和是A 元素的原子序数的4倍,则A、B、C所在的一组是 ( )| A. | Be、Na、Al | B. | P、O、Cl | C. | O、P、Cl | D. | C、Al、P |
分析 A、B、C均为短周期元素,由元素在周期表中的位置,可知A处于第二周期,B、C处于第三周期,令A的原子序数为x,则B原子序数为x+7,C原子序数为x+9,再根据原子序数关系列方程计算确定元素.
解答 解:A、B、C均为短周期元素,由元素在周期表中的位置,可知A处于第二周期,B、C处于第三周期,令A的原子序数为x,则B原子序数为x+7,C原子序数为x+9,B、C元素的原子序数之和是A元素的原子序数的4倍,则:x+7+x+9=4x,解得x=8,故A为O元素,B为P元素,C为Cl元素,
故选:C.
点评 本题考查元素推断,难度不大,根据短周期特点确定元素所在周期,注意掌握同主族元素原子序数关系,利用最外层电子数确定更简单.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生鸡蛋煮熟后,蛋白质发生变性,人食用后,酶不能发挥作用将蛋白质消化,因此生吃鸡蛋比熟吃好 | |
| B. | 登高山时防晒护目是为了防止紫外线引起皮肤和眼睛蛋白质被烧伤变性 | |
| C. | 温度越高,酶对某些化学反应的催化效率越高 | |
| D. | 毛巾、口罩经常用开水蒸煮,被褥放在太阳光下直射,其目的是使油脂水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用空气吹出SO2吸收法从海水中提溴时,直接将海水氯化,然后再进行吹出、吸收可得到溴产品 | |
| B. | 从海水中提取的重水可作原子能反应堆的中子减速剂和传热介质 | |
| C. | 盐田法制盐时,所用的盐田一般分成贮水池、蒸发池、结晶池三部分 | |
| D. | 利用电渗析法,冷冻法制盐,同时也可以得到淡水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
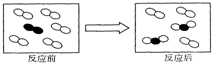
| A. | 反应前容器中的物质为单质 | |
| B. | 反应后容器中的物质为化合物 | |
| C. | 该反应为化合反应 | |
| D. | 该反应由两种反应物反应生成两种生成物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢铁在干燥的环境中不易腐蚀 | |
| B. | 原电池工作时,电解质溶液中的阳离子移向正极 | |
| C. | 用铝质铆钉铆接铁板,铆接处的铁板更易被腐蚀 | |
| D. | 集中回收处理废旧电池的主要目的是防止电池中的重金属离子污染土壤和水源 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 结构或性质信息 |
| X | 原子的L层上s电子数等于p电子数. |
| Y | 原子核外的L层有3个未成对电子. |
| Z | 在元素周期表的各元素中电负性仅小于氟. |
| Q | 单质常温、常压下是气体,原子的M层上有1个未成对的p电子. |
| R | 核电荷数是Y与Q的核电荷数之和 |
| E | 原子序数比R大3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com