
| A�� | 2.4 gþ�ڿ�������ȫȼ������MgO��Mg3N2��ת�Ƶĵ�����Ϊ0.8 NA | |
| B�� | ��״���£�5.6 L������̼�����к��е���ԭ����Ϊ0.5 NA | |
| C�� | 8.7 g MnO2��40 mL 10 mol/L��Ũ�����ַ�Ӧ�����ɵ�����������Ϊ0.1 NA | |
| D�� | 0.1 L 0.5 mol/L CH3COOH��Һ�к��е���������Ϊ0.05 NA |
���� A�����þ�����ʵ�����Ȼ�����þ��Ӧ���Ϊ+2����������
B������n=$\frac{V}{Vm}$���������̼��������ʵ�������϶�����̼���Ӻ���2����ԭ�ӽ��
C����������ֻ����Ũ���ᷴӦ����ϡ�����Ӧ��
D������Ϊ������ʣ����ֵ��룮
��� �⣺A.2.4gþ�����ʵ���Ϊ0.1mol����þ��Ӧ���Ϊ+2�ۣ���0.1molþת��0.2NA�����ӣ���A����
B����״���£�5.6 L������̼�����к��е���ԭ����Ϊ$\frac{5.6L}{22.4L/mol}$��2��NA=0.5 NA����B��ȷ��
C����������ֻ����Ũ���ᷴӦ����ϡ�����Ӧ����Ũ����ܷ�Ӧ��ȫ�������ɵ���������С��0.1NA������C����
D������Ϊ������ʣ����ֵ��룬����0.1 L 0.5 mol/L CH3COOH��Һ�к��е���������С��0.05 NA����D����
��ѡ��B��
���� ���⿼���˰���٤���������йؼ��㣬��ȷ���������Ħ�������ʹ�����������հ���٤�����������ʵ�����Ħ��������������֮���ת����ϵ�ǽ���ؼ���ע������Ũ�ȶԷ�Ӧ��Ӱ�죬��Ŀ�Ѷ��еȣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ƽ��ʱ�������ɵ�ˮ������ȥ�����������HCl��ת���� | |
| B�� | �ں��ݾ��������н���ʱ�����ŷ�Ӧ�Ľ��У������ѹǿһ�����ϼ�С | |
| C�� | ��ѹ�����У���Ӧ��ƽ���ͨ��������壬ƽ�ⲻ�ƶ� | |
| D�� | ƽ��ʱ�������������䣬���������������Ӧ��ƽ�ⳣ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڳ��³�ѹ�£�11.2 LN2���еķ�����Ϊ0.5 NA | |
| B�� | 71gCl2����ԭ����ΪNA | |
| C�� | �ڳ��³�ѹ�£�1molNe���е�ԭ����ΪNA | |
| D�� | ��ͬ�¡�ͬѹ�£���ͬ������κ����嵥��������ԭ������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ�������Һ��ͨ��������Fe2++Cl2=Fe3++2Cl- | |
| B�� | �ں����ҵĽ���Һ������I-���еμ�H2O2�õ�I2��2I-+H2O2+2H+=I2+O2��+2H2O | |
| C�� | ������Һ��ͨ������CO2��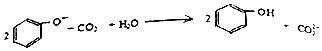 | |
| D�� | ���������Ũ�ȵ�Ba��OH��2ϡ��Һ��NH4HCO3ϡ��Һ��ϣ�Ba2++2OH-+NH4++HCO3-=BaCO3��+NH3•H2O+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
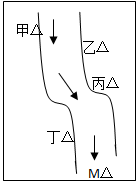 ��һ����Ϻ������С�ӱ��������������ס��ҡ�����������ͼ��ʾ����ͷ��ʾ��ˮ���������ų��ķ�Һ�ÿ������ֻ����Na2CO3��FeCl3��Ca��OH��2��HCl�е�һ�֣�ij��ѧ����С��Ժ�ˮ���ʱ���֣��ټ״���ˮ�����ɫ�����Ҵ���ˮ�ʺ��ɫ���ǣ��۱�����ˮ�ɻ���壬�ܶ����������ݣ���ˮ���壬��M��ˮ����pHС��7��
��һ����Ϻ������С�ӱ��������������ס��ҡ�����������ͼ��ʾ����ͷ��ʾ��ˮ���������ų��ķ�Һ�ÿ������ֻ����Na2CO3��FeCl3��Ca��OH��2��HCl�е�һ�֣�ij��ѧ����С��Ժ�ˮ���ʱ���֣��ټ״���ˮ�����ɫ�����Ҵ���ˮ�ʺ��ɫ���ǣ��۱�����ˮ�ɻ���壬�ܶ����������ݣ���ˮ���壬��M��ˮ����pHС��7���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ӦʽΪMg-2e-�TMg2+ | |
| B�� | �������ܻᷢ������ӦMg+2H2O�TMg��OH��2+H2�� | |
| C�� | ��طŵ�ʱCl-�ɸ���������Ǩ�� | |
| D�� | ������ӦʽΪAgCl+e-�TAg+Cl- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com