
用NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A.在反应KIO3 + 6 HI = KI + 3I2 + 3 H2O中,每生成3mo1 I2转移的电子数为5NA
B.100mL 18.4mo1·L-1硫酸与足量Cu反应,生成SO2的分子数为0. 92NA
C.1 L 0. 1 moI·L-1的CH3COOH溶液中所含的离子和分子总数为0.1NA
D.将0. l mol FeC13滴入沸水中可制得0. 1NA Fe(OH)3胶粒
 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
下列溶液中物质的量浓度为1 mol·L-1的是( )
A.将40 g NaOH溶解在1 L水中
B.将22.4 L HCl气体溶于水配成1 L溶液
C.将1 L 10 mol·L-1的浓盐酸加入9 L水中
D.将10 g NaOH溶解在少量水中,再加蒸馏水直到溶液体积为250 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
卤代烃分子里的卤素原子与活泼金属或其阳离子结合,发生下列反应(X表示卤素原子):
R—X+2Na+X—R′ R—R′+2NaX
R—R′+2NaX
R—X+NaCN R—CN+NaX
R—CN+NaX
根据下列各物质的转化关系填空:

(1)E的结构简式是______________。
(2)B→D的化学方程式是________________________。
(3)C→F的化学方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇是人们开发和利用的一种新能源。已知:
①2H2(g)+O2(g)===2H2O(l)
ΔH1=-571.8 kJ·mol-1;
②CH3OH(g)+1/2O2(g)===CO2(g)+2H2(g) ΔH2=-192.9 kJ·mol-1
(1)甲醇蒸气完全燃烧的热化学方程式为_____________________________________
________________________________________________________________________。
(2)反应②中的能量变化如图所示,则ΔH2=__________。

(3)H2(g)的燃烧热为________。
(4)请你分析H2(g)作为能源比甲醇蒸气作为能源的优点:_____________________
________________________________________________________________________(写出两点即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于0.1mol/LNa2CO3溶液的叙述错误的是 ( )
A.0.5L该溶液中钠离子的物质的量浓度为0. 05mol/L
B.1L该溶液中含有Na2CO3的质量为10.6g
C.从1L该溶液中取出100mL,则取出溶液中Na2CO3的物质的量浓度为0.1mol/L
D.取该溶液10mL,加水稀释至100mL后,Na2CO3的物质的量浓度为0.01mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验设计或实验操作中,正确的是 ( )
 | |||
 |
A.铜与浓硝酸反应制取NO2 B.该装置设计合理,可实现石油的分馏
 |

C.称量25g氢氧化钠 D.H2O2溶液与MnO2制备O2
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E是五种短周期的主族元素,它们的原子序数依次增大,A、D都能与C按原子个数比为1:1或2:1形成化合物,A、B组成的气态化合物的水溶液呈碱性,E与C的最外层电子数相同。
(1)画出D的原子结构示意图 ,E元素在周期表中的位置是 。
(2)A与C形成的化合物中,原子个数比为1:1的化合物的结构式为 。
(3)D与C按原子个数比为1:1形成化合物的电子式是 。
(4)B、C所形成氢化物的稳定性由强到弱的顺序是 、 (填具体的化学式)。
(5)F是一种历史悠久、应用广泛的金属元素。若将F金属投入到盐酸溶液中,生成了浅绿色溶液M。写出M的酸性溶液和A与 C形成的一种化合物反应的离子方程式:
。
(6)有人设想寻求合适的催化剂和电极材料,以A2、B2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极电极反应式:
;放电时溶液中H+移向 (填“正”或“负”)极。
(7) E(s)+O2(g) EO2(g) △H1 E(g)+O2(g) EO2(g) △H2,
则△Hl △H2(填“>”或“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
聚酰胺-66常用于生产帐蓬、渔网、降落伞及弹力丝袜等织物,可利用下列路线合成:

(1)能与银氨溶液反应的B的同分异构体的结构简式为________。
(2)D的结构简式为________;①的反应类型为________。
(3)为检验D中的官能团,所用试剂包括NaOH水溶液及________。
(4)由F和G生成H的反应方程式为_____________________ ___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
结晶玫瑰是具有强烈玫瑰香气的香料,可由下列反应路线合成(部分反应条件略去):

(1)A的类别是________,能与Cl2反应生成A的烷烃是________;B中的官能团是________。
(2)反应③的化学方程式为____________________。
(3)已知:B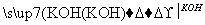 苯甲醇+苯甲酸钾,则经反应路线①得到的产物加水萃取、分液,能除去的副产物是________。
苯甲醇+苯甲酸钾,则经反应路线①得到的产物加水萃取、分液,能除去的副产物是________。
 | |||
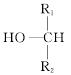 | |||
 (4)已知: +
(4)已知: + 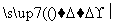 +H2O,则经反应路线②得到一种副产物,其核磁共振氢谱有4组峰,各组吸收峰的面积之比为________。
+H2O,则经反应路线②得到一种副产物,其核磁共振氢谱有4组峰,各组吸收峰的面积之比为________。
(5)G的同分异构体L遇FeCl3溶液显色,与足量饱和溴水反应未见白色沉淀产生,则L与NaOH的乙醇溶液共热,所得有机物的结构简式为________。(只写一种)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com