
下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),生成物并不改变的是
A.Na和O2 B.NaOH和CO2 C.Na2O2和CO2 D.NaAlO2和HCl
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
按要求回答下列问题:
(1) 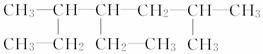 的名称为____________________。
的名称为____________________。
(2)A、B、C三种烃的化学式均为C6H10,它们的分子中均无支链或侧链。
①若A为环状,则其结构简式为________________。
②若B为含有双键的链状结构,且分子中不存在“ ”基团,则其可能的结构简式为________________________________(任写一种)。
”基团,则其可能的结构简式为________________________________(任写一种)。
③若C为含有三键的链状结构,则其可能的结构简式及名称为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
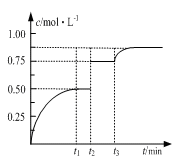
一定温度下,将1molM和1molN气体充入2L恒容密闭容器,发生反应M(g)+ N(g) xP(g)+Q(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体P的浓度随时间变化如图所示。下列说法正确的是( )
xP(g)+Q(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体P的浓度随时间变化如图所示。下列说法正确的是( )
A.反应方程式中的x=1
B.t2时刻改变的条件是使用催化剂
C.t3时刻改变的条件是移去少量物质Q
D.t1~t3间该反应的平衡常数均为4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于氯气或氯水的叙述不正确的是
A.氯气能使润湿的淀粉碘化钾试纸变蓝
B.新制的氯水呈黄绿色是因为在溶液中溶有氯气分子
C.与久置氯水不同,在新制氯水中加入硝酸银溶液后无白色沉淀
D.氯水久置后,会使溶液酸性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应的实质和相应的规律是
A.化合价的升降,化合价的升高和降低的总数相等
B.电子的转移,得电子总数和失电子总数相等
C.得氧和失氧,氧原子数目不变
D.物质的种类发生改变,质量守恒定律
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应在工农业生产和日常生活中有广泛运用。
(1)罐头厂在装食物罐头时通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类防腐剂应具有 ▲ 。 (填“氧化性”或“还原性”);
(2)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,Fe2+更
容易被吸收。服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中维生素C所起的作用是 ▲ 。(填“氧化作用”或“还原作用”);
(3)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式,而硫酸铁则无这种药效。用硫酸
亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是 ▲ 。
(4)在下列的空白处填写最适宜的除杂试剂,并写出相应的离子方程式
① FeCl2中含少量FeCl3杂质 ▲ , ▲ 。
② FeCl3中含少量FeCl2杂质 ▲ , ▲ 。
③ FeSO4中含少量CuSO4杂质 ▲ , ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
阿伏加德罗常数约为6.02×1023mol—1,下列叙述中正确的是( )
A.常温常压下,18.0 g重水(D2O)所含的电子数约为10×6.02×1023
B.室温下,42.0 g乙烯和丙烯的混合气体中含有的碳原子数约为3×6.02×1023
C.标准状况下,22.4 L苯所含的分子数约为6.02×1023
D.标准状况下,a L乙烷气体中的所含共价键数约为(a/22.4)×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量的铁与1L含0.4molHNO3的溶液恰好完全反应生成NO,则被还原的HNO3的物质的量为( )
A.0.4mol B.0.3mol C.0.lmol D.条件不足,无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
在0.1 mol·L-1CH3COOH溶液中存在如下电离平衡:CH3COOHCH3COO-+H+,对于该平衡下列叙述正确的是( )
A.加入水时,平衡逆向移动
B.加入少量NaOH固体,平衡正向移动
C.加入少量0.1 mol·L-1盐酸,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡正向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com