
| A. | ②④⑦ | B. | ①②⑦ | C. | ①④⑤ | D. | ②⑥⑦ |
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 58.5g NaCl溶于1L水中配得1mol/L NaCl溶液 | |
| B. | 在标准状况下,44.8LHCl气体溶于水配成1L溶液,所得溶液中溶质的物质的量浓度为2mol/L | |
| C. | 在标准状况下,22.4L氨气溶于水配成1L溶液,从所得溶液中取出10mL,其物质的量浓度为1mol/L | |
| D. | 1mol/L的CaCl2溶液1L,取出100mL,含0.2molCl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或者增大压强,速率的变化都符合的示意图的反应是( )
如图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或者增大压强,速率的变化都符合的示意图的反应是( )| A. | 2SO2(g)+O2(g)?2SO3(g) H<0 | B. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g) H<0 m | ||
| C. | H2(g)+I2(g)?2HI(g) H>0 | D. | N2(g)+3H2(g)?2 NH3(g) H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | XX′n 属于活泼非金属单质 | |
| B. | ICl3 属于共价化合物 | |
| C. | 上述反应中HCl是还原产物 | |
| D. | ICl溶于水的反应:ICl+H2O=HIO+HCl 不属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
实验I: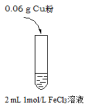 | 实验现象 |
| i.加入Cu粉后充分振荡,溶液变成浅蓝绿色; ii.取少量i中清液于试管中,滴加2滴1 mol/L KSCN溶液,立即出现白色沉淀,溶液变为红色,振荡后红色迅速褪去;继续滴加KSCN数滴溶液后,溶液又变为红色 |
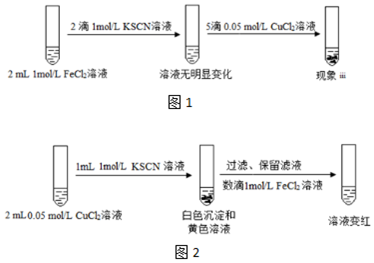
| 实验IV | 现象 |
| 向2mL 1mol/LFeCl3溶液中加入1滴1mol/L KSCN溶液,再加入足量的Cu粉 | 充分振荡,溶液红色褪去,有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①和⑤ | B. | ②和③ | C. | ③⑤和⑥ | D. | ④和⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
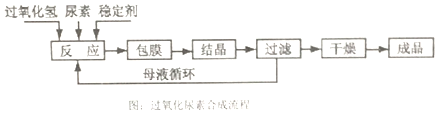
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
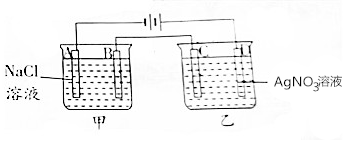 按如图进行电解实验(A,B,C,D均为惰性电极).
按如图进行电解实验(A,B,C,D均为惰性电极).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
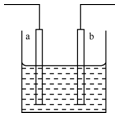
| A. | a,b可能是同种材料的电极 | |
| B. | 该装置可能是电解池,电解质溶液为稀硝酸 | |
| C. | 该装置可能是原电池,电解质溶液为稀盐酸 | |
| D. | 该装置可看作是铜一锌原电池,电解质溶液是稀硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com