
归纳法是高中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结:归纳正确的是
①向0.1 mol·L-1 CH3COOH溶液中加入少量冰醋酸,平衡向正反应方向移动,电离程度增大;
②常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则有c(Na+) +c(H+)=c(OH-)+c(CH3COO-)
+c(H+)=c(OH-)+c(CH3COO-)
③常温下,AgCl在同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同;
④常温下,已知醋酸电离平衡常数为Ka;醋酸根水解平衡常数为Kh;水的离子积
A.①②④ B.②④ C.②③ D.①②③④
科目:高中化学 来源:2016-2017学年山东省滨州市邹平县高二上学期期中化学试卷(解析版) 题型:填空题
下面是新设的一组垃圾箱的说明
滨州市生活垃圾分类 | ||
可回收垃圾 |
| 有害垃圾 |
1. 纸类 2.玻璃 3.金属 4.塑料 5.橡胶 6.纺织品 | 1. 厨房垃圾 2.灰土 3.杂草 4.枯枝 5.花卉 |
2.电池 3.喷雾罐 4.指甲油瓶 5.药品药瓶 6.涂改液瓶 |
(1)小明在整理房间时,清理出如下物品,它们应分别放入哪个垃圾箱(请填序号):A.废作业本;B.汽水易拉罐;C.生锈铁钉;D.矿泉水瓶;E.烂苹果;F.涂改液瓶
应放入“可回收垃圾箱”的是 ;
应放入“不可回收垃圾箱”的是 ;
应放入“有害垃圾箱”的是 。
(2)小明用盐酸除去铁钉上的锈(主要成分为氧化铁)以重新使用它,请写出盐酸除锈的化学方程式 。
(3)废铜有两种回收方法:
方法一:Cu+4HNO3=Cu(NO3)2+2X↑+2H2O(X是一种大气污染物)
方法二:铜在空气中加热生成氧化铜,氧化铜再与盐酸反应生成氯化铜和水。
①方法一中,X的化学式为 ;
方法二的优点是 ;
②请写出从氯化铜溶液中提取铜的化学方程式____________________,该反应属于化学反应的基本类型是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二上学期期中化学试卷(解析版) 题型:选择题
下列关于盐酸与醋酸两种稀溶液的说法正确的是( )
A.相同浓度的两溶液中c(H+)相同
B.100mL 0.1mol/L的两溶液能中和等物质的量的氢氧化钠
C.pH=2的两溶液稀释后pH仍相同,盐酸稀释的程度大于醋酸稀释的程度
D.两溶液中分别加入少量对应的钠盐固体,c(H+)均明显减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学试卷(解析版) 题型:选择题
已知:氢氧化镁能溶于浓度均为3mol/L的①盐酸②NH4Cl溶液③醋酸铵溶液(中性),下列说法正确的是( )
A.c(NH4+):③>②
B.pH:①>②>③
C.Mg(OH)2溶于②的主要原因是由于NH4+水解使溶液显酸性,导致平衡Mg(OH)2(s) Mg2+(aq)+2OH-(aq)向溶解方向移动
Mg2+(aq)+2OH-(aq)向溶解方向移动
D.等体积①和③混合溶液中c(Cl-)>c(NH4+)>c(H+)>c(CH3COO-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学试卷(解析版) 题型:选择题
室温时,CaCO3在水中的溶解平街曲线如图所示。已知25℃ 其浓度积为2.8×10-9mol2/L2,下列说法不正确的是( )
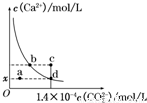
A.x数值为2×10-5 B.c点时有碳酸钙沉淀生成
C.加入蒸馏水可使溶液由d 点变到a点 D.b点与d对应的溶度积相等
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上期中化学卷(解析版) 题型:填空题
在25℃时,2L的密闭容器中A、B、C三种气体的初始浓度和平衡浓度如下表:
物质 | A | B | C |
初始浓度/mol·L-1 | 1.0 | 2.0 | 0 |
2min时,平衡浓度/mol·L-1 | 0.4 | 0.2 | 1.2 |
请填写下列空白:
(1)该反应方程式可表示为: ;反应达平衡时,A的转化率为___________。
(2)从反应开始到达化学平衡,生成C的平均反应速率为 ;25℃时,反应的化学平衡常数K值(数值)为_____________。
(3)能判断该反应已达到化学平衡状态的依据是__________。
a.容器内压强不变
b.混合气体的密度不变
c.3v正(B)=2v逆(C)
d.c(A)=c(C)
e.混合气体的平均相对分子质量不变
(4)若已知该反应为放热反应,下图表示由于条件改变而引起反应速度和化学平衡的变化情况:
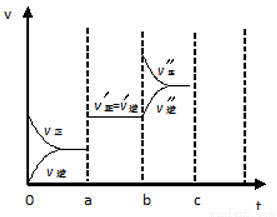
a 点时改变的条件可能是 ;b点时改变的条件可能是 。





 (5)如果上述反应起始是按“1 mol A+3 mol B”充入,达平衡时C的浓度为a mol/L;维持容器体积和温度不变,按下列方法改变起始物质的量,达到平衡时C的浓度仍为a mol/L的是 (填序号)
(5)如果上述反应起始是按“1 mol A+3 mol B”充入,达平衡时C的浓度为a mol/L;维持容器体积和温度不变,按下列方法改变起始物质的量,达到平衡时C的浓度仍为a mol/L的是 (填序号)
①2 mol A+6 mol B ②2mol C ③4mol C ④0.5 mol A+1.5mol B+1 mol C
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上期中化学卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中能大量共存的是( )
A.H2O2的溶液中:Na+,F-,SO32-;
B.c(OH-)/c(H+)=1012的溶液中:Fe2+、NO3-、SO42-、Na+;
C.由水电离的c(H+)=1×10-14mol·L-1的溶液中:K+、Ba2+、Cl-、NO3-;
D.pH=1的溶液中:Na+,K+,Cl-,S2O32-;
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省嘉兴市七校高一上期中化学试卷(解析版) 题型:实验题
实验室常用二氧化锰和浓盐酸共热的方法制取氯气,反应中二氧化锰被还原为MnCl2。根据要求回答下列问题:
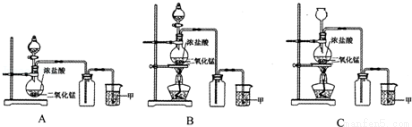
(1)A、B、C三套装置中,应选用的装置是 (选填“A”、“B”、“C”)。
(2)写出实验室用上述方法制取氯气的化学方程式 。
(3)为了防止氯气污染环境,图中所示的溶液甲为 ,在该溶液中发生反应的化学方程式 。
(4)利用该原理和装置进行实验,制得的氯气中往往含有的杂质有 ,可依次通入到 除去。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市武清区等五区县高二上期中化学卷(解析版) 题型:选择题
已知热化学方程式:则下列说法正确的是
①CO(g)+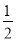 O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
②H2(g)+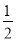 O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
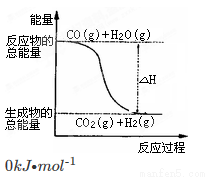
A.H2的燃烧热为241.8kJ·mol -1
B.由反应①、②可知如图所示的热化学方程式为 CO(g)+H2O(g)=CO2(g)+H2(g) ΔH =-41.2kJ·mol -1
C.H2(g)转变成H2O(g)的化学反应一定要释放能量
D.根据②推知反应H2(g) +1/2O2(g)=H2O(l):ΔH>-241.8 kJ·mol -1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com