
【题目】下列说法符合事实的是
A.物质的量浓度相同的硫酸氢铵溶液和醋酸铵溶液中,硫酸氢铵中的铵根离子物质的量浓度较小
B.在10mL 0.1 mol/L的AgNO3溶液中加入6mL等浓度的NaCl溶液,有白色沉淀产生,再加入6 mL等浓度的Na2S溶液,溶液中又有黑色沉淀生成,说明Ksp(Ag2S)< Ksp(AgCl)
C.物质的量浓度均为0.02 mol/L的弱酸HX及其盐NaX等体积混合后:c(X-)+ c(HX)= 0.02 mol/L
D.己知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12。在含C1-、CrO42-浓度相同的溶液中滴加AgNO3溶液时,首先生成Ag2CrO4沉淀。
【答案】C
【解析】
试题分析:A、硫酸氢铵溶液中电离出的氢离子抑制铵根水解,醋酸铵溶液中醋酸根促进铵根水解,则硫酸氢铵中的铵根离子物质的量浓度较大,A错误;B、由于反应中硝酸银过量,所以再加入硫化钠溶液中一定产生硫化银沉淀,所以不能说明二者的溶度积常数大小关系,B错误;C、根据物料守恒可知物质的量浓度均为0.02 mol/L的弱酸HX及其盐NaX等体积混合后:c(X—)+ c(HX)= 0.02 mol/L,C正确;D、在含C1-、CrO42-浓度相同的溶液中滴加AgNO3溶液时,根据二者的溶度积常数可知沉淀时需要银离子的浓度分别是![]() ,所以首先生成AgCl沉淀,D错误,答案选C。
,所以首先生成AgCl沉淀,D错误,答案选C。


 小学教材全测系列答案
小学教材全测系列答案科目:高中化学 来源: 题型:
【题目】以乙烯为原料合成化合物C的流程如图所示:
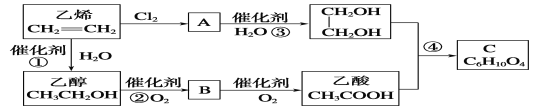
(1)A和B中含有的官能团名称分别为___ _____,____________。
(2)写出A的结构简式:____________ ___________。
(3)①③的反应类型分别为______ __反应和____ ____反应。
(4)写出乙醇的同分异构体的结构简式:______________ ______。
(5)写出反应②和③的化学方程式:
②____________________________;④_____________________________。
(6)写出B与新制Cu(OH)2悬浊液反应的化学方程式:_____ ___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修2:化学生活与技术]以黄铁矿为原料,采用接触法生产硫酸的流程可简示如下:
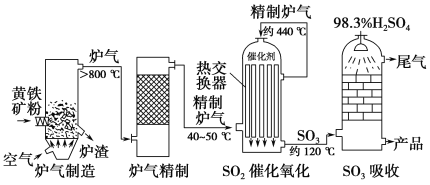
请回答下列问题:
(1)在炉气制造中,生成SO2的化学方程式为_________________________________________;
(2)炉气精制的作用是将含SO2的炉气________、________及干燥,如果炉气不经过精制,对SO2催化氧化的影响是___________________________________________;
(3)精制炉气(含SO2体积分数为7%、O2为11%、N2为82%)中SO2平衡转化率与温度及压强关系如下图所示。在实际生产中,SO2催化氧化反应的条件选择常压、450 ℃左右(对应图中A点),而没有选择SO2转化率更高的B或C点对应的反应条件,其原因分别是____________。
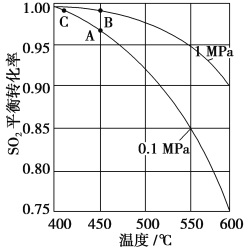
(4)在SO2催化氧化设备中设置热交换器的目的是________,从而充分利用能源。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99kJ·mol-1。请回答下列问题:

(1)图中A表示 E的大小对该反应的反应热 (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点 (填“升高”还是“降低”),△H (填“变大”、“变小”或“不变”),
(2)图中△H= KJ·mol-1;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、白藜芦醇的结构简式如下图。它广泛存在于食物(如桑椹、花生,尤其是葡萄)中,可能具有抗癌性。下列有关白藜芦醇的说法正确的是
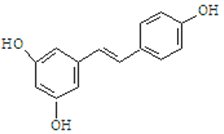
A.该有机物属于醇类
B.1mol该有机物与H2加成时最多消耗1mol H2
C.1mol该有机物与Br2反应时最多消耗6mol Br2
D.1mol该有机物最多消耗3mol NaOH
Ⅱ、根据下列的有机物合成路线回答问题:

(1)写出A、B的结构简式:A 、B 。
(2)写出各步反应类型:
① 、② 、③ 。
(3)写出②、③的反应方程式:
②
③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某实验室要用90mL1.00 mol·L-1的NaOH溶液。在配制该NaOH溶液的过程中:
①除了要使用托盘天平、药匙、烧杯、玻璃棒、胶头滴管,还要使用的仪器有 。
②需用托盘天平称取NaOH的质量为 g。
(2)从海带中提取碘的流程如下图:

①指出提取碘的过程中实验操作、操作的名称:c__________
②在3mL碘水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象是
。(注:下图试管中深色区为紫红色溶液)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C三种烃,其球棍模型如下图:
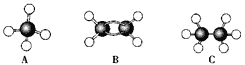
(1)等质量的以上物质完全燃烧时耗去O2的量最多的是________(填对应字母,下同);
(2)同状况、同体积的以上三种物质完全燃烧时耗去O2的量最多的是____________;
(3)等质量的以上三种物质燃烧时,生成二氧化碳最多的是________,生成水最多的是________。
(4)在120℃、1.01×105 Pa下时,有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)如图为1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图。已知E1=134KJ/mol,E2=368KJ/mol( E1、 E2为反应的活化能)。若在反应体系中加入催化剂,反应速率增大,则E1、△H的变化分别是 、 (填“增大”、“减小”或“不变”)。写出该 反应的热化学方程式 。
(2)若反应SO2(g)+I2(g)+2H2O(g)=H2SO4(l)+2HI(g)在150℃下能自发进行,则△H___0。
A.大于 B.小于 C.等于 D.大于或小于都可

Ⅱ.以CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取乙醇的反应:
2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)
CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)
在密闭容器中,按CO2与H2的物质的量之比为1:3进行投料,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(y%)如下图所示。完成下列填空:
(1)表示CH3CH2OH体积分数曲线的是____(选填序号)。
(2)在一定温度下反应达到平衡的标志是 。
A.平衡常数K不再增大
B.CO2的转化率不再增大
C.混合气体的平均相对分子质量不再改变
D.反应物不再转化为生成物
(3)其他条件恒定,达到平衡后,能提高H2转化率的措施是_______(选填编号)。
A.升高温度 B.充入更多的H2 C.移去乙醇 D.增大容器体积
(4)图中曲线a和c的交点R对应物质的体积分数yR=_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有X、Y、Z三种元素,已知有如下情况:
①X、Y、Z的单质在常温下均为气体。
② X的单质在Z的单质中燃烧,生成XZ,燃烧时火焰呈苍白色。
③ XZ极易溶于水,在水溶液中电离出X+和Z-。XZ的水溶液可使石蕊试液变红。
④两分子X的单质可与一分子Y的单质化合生成两分子X2Y,X2Y常温下为液体。
⑤ Z的单质溶于X2Y中,所得溶液具有漂白作用。
请完成下列问题:
(1)写出XZ和X2Y的化学式:XZ X2Y
(2)Z的单质溶于X2Y后,溶液起漂白作用的物质是 (写化学式)。
(3)写出实验室制取X的单质的离子方程式 _______________。
(4)Z的单质能否与氢氧化钠溶液发生反应: (填“能”或“否”),若能,请写出反应的离子方程式: _______________。
(若不能反应,则此空不必填写)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com