
【题目】常温下,现有![]() 溶液,
溶液,![]() 已知含氮
已知含氮![]() 或含碳
或含碳![]() 各微粒的分布分数
各微粒的分布分数![]() 平衡时,各微粒浓度占总微粒浓度之和的分数
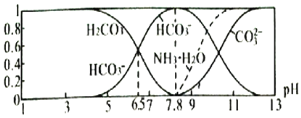
平衡时,各微粒浓度占总微粒浓度之和的分数![]() 与pH的关系如图所示。下列说法正确的是
与pH的关系如图所示。下列说法正确的是![]()
A.当![]() 时,溶液中存在下列关系:
时,溶液中存在下列关系:![]()
![]()
B.![]() 溶液中存在下列关系:
溶液中存在下列关系: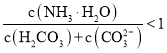
C.向![]() 的上述溶液中逐滴滴加氢氧化钠溶液时,
的上述溶液中逐滴滴加氢氧化钠溶液时,![]() 和
和![]() 浓度逐渐减小
浓度逐渐减小
D.分析可知,常温下水解平衡常数![]() 的数量级为
的数量级为![]()
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在P+CuSO4+H2O→Cu3P+H3PO4+H2SO4(未配平)的反应中,7.5 mol CuSO4可氧化P的物质的量为________mol。生成1 mol Cu3P时,参加反应的P的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述中,合理的是
A.用已知浓度的NaOH溶液测定盐酸的浓度,酸式滴定管未用待装溶液润洗会造成测定结果偏高
B.![]() 溶液中:
溶液中:![]()
C.等体积等浓度的氢氧化钠与醋酸混合:![]()
D.![]() 相等的
相等的![]() 溶液、
溶液、![]() 溶液和
溶液和![]() 溶液:
溶液:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法不正确的是( )
A.用来制造电线电缆的聚乙烯树脂属于热塑性高分子材料
B.研发可降解高分子材料,可以减少“白色污染”
C.棉、麻、羊毛及合成纤维完全燃烧都只生成![]() 和
和![]()
D.硅橡胶![]() 可由
可由![]() 经水解、缩聚两步反应制得
经水解、缩聚两步反应制得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是![]()
A.![]() 有机物
有机物![]() 的分子结构中含有的
的分子结构中含有的![]() 键数目一定为
键数目一定为![]()
B.一定温度下,氯化铵水解离子方程式:![]() ,若用
,若用![]() 表示的离子积,
表示的离子积,![]() 表示氨水电离常数,则氯化铵水解平衡常数
表示氨水电离常数,则氯化铵水解平衡常数![]()
C.已知反应:![]() :
:![]() :
:![]() ;则在酸性溶液中氧化性:
;则在酸性溶液中氧化性:![]()
D.已知
共价键 |
|
|
|
|
键能 | 360 | 436 | 431 | 176 |
则反应![]() 的焓变为:
的焓变为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应 A(g)+3B(g)![]() 2C(g)+2D(g),在不同情况下,测得有下列四个反应速率,其反应速率最快的是( )
2C(g)+2D(g),在不同情况下,测得有下列四个反应速率,其反应速率最快的是( )
A.υ(A)=0.2molL﹣1s﹣1B.υ(B)=0.6molL﹣1s﹣1
C.υ(C)=0.6molL﹣1s﹣1D.υ(D)=0.5molL﹣1s﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是从海藻灰和智利硝石矿层中提取碘的主要反应:①2NaI+MnO2+3H2SO4===2NaHSO4+MnSO4+2H2O+I2 ;②2NaIO3+5NaHSO3===2Na2SO4+3NaHSO4+H2O+I2下列说法正确的是( )
A. 氧化性:MnO2>SO![]() >IO
>IO![]() >I2
>I2
B. I2在反应①中是还原产物,在反应②中是氧化产物
C. 反应①②中生成等量的I2时转移电子数之比为1∶5
D. NaHSO3溶液呈酸性,NaHSO3溶液中c(HSO![]() )>c(H2SO3)>c(SO
)>c(H2SO3)>c(SO![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:

(1)该反应为________反应(填“放热”或“吸热”)。
(2)A和B的总能量比C和D的总能量_________(填“高”或“低”)。
(3)该反应的物质中的化学能通过化学反应转化成________释放出来。
(4)该反应的反应物化学键断裂吸收的能量________(填“高”或“低”)于生成物化学键形成放出的能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)Cu(NO3)2的水溶液呈______(填“酸”、“中”、“碱”)性,常温时的pH _____7(填“>”、“=”、“<”), 原因是(用离子方程式表示):_______________________________
(2)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是________ ,把Al2(SO4)3溶液蒸干得到的固体产物是___________ 。
(3)在Na2S溶液中存在的电荷守恒式为____________物料守恒式为___________质子守恒式为________________
(4)泡沫灭火器的原理(药品:Al2(SO4)3溶液、NaHCO3溶液)原理为___________用离子方程式解释)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com