
| A��2CH4(g)+4O2(g)��2CO2(g)+4H2O(l) ��H=+890kJ/mol |
| B��CH4(g)+2O2(g)��CO2(g)+2H2O(l) ��H=+890kJ/mol |
| C��CH4(g)+2O2(g)��CO2(g)+2H2O(l) ��H=-890kJ/mol |
| D��1/2 CH4(g)+ O2(g)��1/2CO2(g)+ H2O(g) ��H=-890kJ/mol |
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��2C2H6(g)+7O2 (g) = 4CO2 (g)+6H2O(l)����H=��1190kJ/mol |
| B��C2H6(g)+7/2O2 (g) =2CO2 (g)+3H2O(g)����H=��1190kJ/mol |
| C��298k��101kPaʱ��30g����������ȫȼ������CO2�����Һ̬ˮ���ų�1190kJ������ |
| D���÷�Ӧ�У���Ӧ�������е�������С�������������е��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
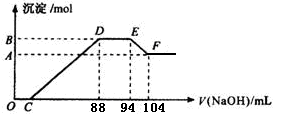
| A������ƿ�к�����������ˮ���ᵼ���������Һ��Ũ��ƫС |
| B��������Һʱ�����ڶ���ʱ���Ӷ������ᵼ���������Һ��Ũ��ƫ�� |
| C���к͵�����������ʵ�����Ũ�ȵ�����ʹ��������ĵ�n(NaOH)��� |
| D��25����60��ʱ��ˮ��pH��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��95�洿ˮ��pH<7��˵�����ȿɵ���ˮ������ |
| B�������£�pH��3�Ĵ�����Һ��ϡ����10����pH��4 |
| C�������£�0.2mol��L�����ᣬϡ����2����pH��l |
| D�������£�pH=3�Ĵ�����Һ����pH��11������������Һ�������Ϻ�pH��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������������HNO3������NH4��ˮ�� |
| B�����������İ�ˮ��ʹ��Һ��pH����7 |
| C������������NH4NO3 |
| D������������NaOH��ʹ��Һ��pH����7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��14 | B��15 | C��13 | D������ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ȡ� | B������������Һ | C����������������Һ | D������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
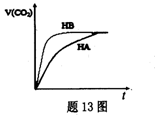
| A����Ӧ����������Һ��c(Aһ��> c��B���� |
| B��pH=5.3��NaA��HA�Ļ����Һ�У�c��Na+��<c��Aһ�� |
| C���к������ͬ��pH��ͬ��HA��HB��Һ��������NaOH�����ʵ������߶� |
| D����ͬ���ͬŨ�ȵ�NaA��NaB��Һ��ǰ�ߵ����������Ⱥ��߶� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com