
【题目】COCl2 (g) ![]() CO(g)+Cl2 (g) △H>0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO 的浓度 ④加催化剂 ⑤恒压通入惰性气体,能提高COCl2 转化率的是( )
CO(g)+Cl2 (g) △H>0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO 的浓度 ④加催化剂 ⑤恒压通入惰性气体,能提高COCl2 转化率的是( )
A.①⑤ B.①② C.③⑤ D.②④
科目:高中化学 来源: 题型:
【题目】莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机化合物的说法正确的是( )
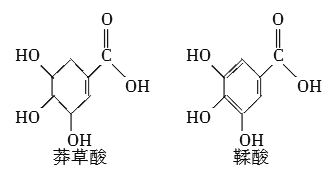
A.两种酸都能与溴水发生加成反应
B.两种酸与三氯化铁溶液都能发生显色反应
C.鞣酸分子与莽草酸分子相比多了两个碳碳双键
D.等物质的量的两种酸与足量的金属钠反应产生氢气的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某非金属单质A经下图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:
![]()
(1)若A常温下为淡黄色固体,B是无色有刺激性气味气体。
①D的化学式:_______;
②写出B→C反应的化学方程式:_________________;
③氯水和B皆可作漂白剂。若同时使用于漂白一种物质时,其漂白效果是_______(填“增强”“减弱”“不变”),用离子方程式解释上述原因_______________。
(2)若A是一种能使湿润的红色石蕊试纸变蓝的气体,C是红棕色气体。
①A、C的化学式分别是:A_______,C_____________;
②写出A→B反应的化学方程式:___________________;
③D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中石化于2012年将年产120万吨的乙烯工程落户大庆,乙烯是有机化工工业的重要原料,有很多重要用途。如:乙烯催化氧化成乙醛可设计成如下图所示的燃料电池,在制备乙醛的同时还可获得电能,其总反应化学方程式为:2CH2=CH2+O2→2CH3CHO。下列有关说法正确的是
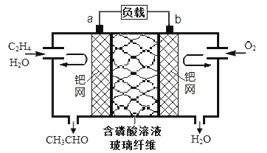
A. 该电池电极a为正极,b为负极
B. 电子移动方向:电极a→磷酸溶液→电极b
C. 负极反应式为:CH2=CH2-2e-+H2O=CH3CHO+2H+
D. b电极有2.24LO2反应,溶液中有0.4molH+迁移到b电极上反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.
硫代硫酸钠是一种重要的化工产品,某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。
I.[查阅资料]
(1)Na2S2O3·5H2O是无色透明晶体,易溶于水,受热、遇酸均反应,其稀溶液与BaCl2溶液混合无沉淀生成。
(2)向Na2CO3和Na2S混合液中通入SO2可制得Na2S2O3,所得产品常含有少量Na2SO3和Na2SO4。
(3)Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl。
Ⅱ.[制备产品]实验装置如图所示(省略夹持装置):
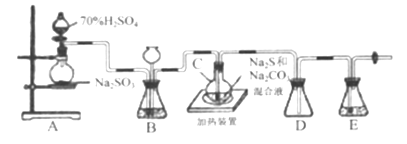
烧瓶C中发生反应如下:
Na2CO3(aq)+SO2(g)=Na2SO3(aq)+CO2(g)
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l)
S(s)+Na2SO3(aq)![]() Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
(1)检查装置气密性。仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若__________,则整个装置气密性良好:装置E的作用是__________。
(2)按图示加入试剂。向A中烧瓶滴加浓H2SO4,产生的气体将装置中空气排尽后,再加热C,A中反应的化学方程式是______;为提高产品纯度,应使C中Na2CO3和Na2S恰好完全反应,则C烧瓶中Na2CO3和Na2S物质的量之比为_______ 。
(3)装置B的另一作用是观察SO2的生成速率,其中的液体最好选择_____。
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
实验中要控制SO2生成速率,使SO2缓慢进入C中可采取的措施有_______;为了保证硫代硫酸钾的产量,该实验一般控制在碱性环境下进行。否则产品发黄,原因是______。
(4)等Na2S和Na2CO3完全消耗后,结束反应。趁热过滤C中混合物,将滤液水浴加热浓缩、_____,经过滤、洗涤、干燥,得到产品。
Ⅲ.[探究与反思]
为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,_____(所需试剂从稀HNO3、稀H2SO4、稀HCl、蒸馏水中选择),若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 溶解度大的化合物一定是强电解质
B. 胶体与溶液的本质区别是分散剂粒子大小的不同
C. 物质在发生化学反应的过程中,都伴随着能量的变化
D. 金属的冶炼必须在高温下进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定质量CaCl2和HCl的混合溶液中逐滴加入浓度为1.000 mol·L-1的Na2CO3溶液,反应过程中加入的Na2CO3溶液的体积与产生沉淀或气体的质量关系如图所示。
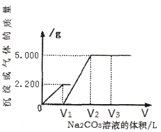
(1)样品中物质的量之比n (CaCl2) :n(HCl)=_____________。
(2)V2=_____________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中发生反应:xA(g)+B(g)![]() 2C(g) △H<0,A、C的物质的量随时间变化的关系如右表所示。下列有关说法正确的是
2C(g) △H<0,A、C的物质的量随时间变化的关系如右表所示。下列有关说法正确的是

A. x=1
B. 反应开始2min内,用B表示的反应速率为0.05mol · L-l · min -1
C. 反应进行到lmin时,反应体系达到化学平衡状态
D. A的正反应速率等于C的逆反应速率时,反应体系达到化学平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质与用途具有对应关系的是
A. 常温下铁能被浓硝酸钝化,可用铁制容器贮运浓硝酸
B. 明矾溶于水能形成胶体,可用于自来水的杀菌消毒
C. 浓硫酸有吸水性,可用于干燥二氧化硫和氨气
D. 金属钠具有强还原性,可与TiCl4溶液反应制取金属Ti
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com