
已知A.B.C.D.E是短周期中原子序数依次增大的5种元素,B.C同周期,D.E也同周期,D原子最外层电子数与最内层电子数相等,A.B.C.D的原子序数之和是E的两倍,D与C形成的化合物是一种耐高温材料,A.B形成的气态化合物的水溶液呈碱性。下列说法正确的是
A.原子半径:D>B>E>C>A B.单质D可用海水作原料获得
C.热稳定性:EA4>A2C D.化合物DC与化合物EC2中化学键类型相同
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )。
①Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
②Na2CO3溶液和NaHCO3溶液都能跟CaCl2溶液反应得到白色沉淀
③钠在常温下不容易被氧化
④Na2O2可作供氧剂,而Na2O不行
⑤向石蕊试液中加入Na2O2粉末,溶液先变蓝后褪色,并有气泡生成
⑥钠与浓NH4Cl溶液反应,放出的气体中含H2和NH3
A.都正确 B.②③④⑤
C.②⑤⑥ D.④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
一家制药公司首次在网站上悬赏下列化合物的合成路线,该化合物的结构如图所示:
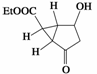
试回答下列问题:
(1)上述结构简式中Et表示乙基,该分子的化学式为________________,有机物归类时,母体优先顺序为酯>酸>醛(或酮)>醇等,则该分子所属类别是________________。
(2)解决有机物分子结构问题的手段之一是核磁共振,下图是计算机软件模拟出的该分子氢原子的核磁共振波谱图。氢原子在分子中的化学环境(原子之间相互作用)不同,其峰线在核磁共振谱图中就处于不同的位置;化学环境相同的氢原子越多,峰线的强度(高度)越大。
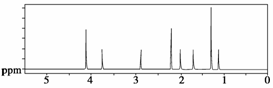
试参考该分子的结构简式分析谱图:该分子中共有______种化学环境不同的氢原子;谱线最高者表示有________个化学环境相同的氢原子;谱线最低者表示有________个化学环境相同的氢原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
取ag某物质在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应.反应后增加的固体的质量小于ag。下列物质中能满足上述结果的是
A.H2 B.CO C.C2H2O4 D.C12H22O11
查看答案和解析>>
科目:高中化学 来源: 题型:
人们对未发现的第114号元素很感兴趣,预测它有良好的力学.光学.电学性质,它被命名为“类铅”。以下对“类铅”的叙述正确的是
A.最外层有6个电子
B.位于元素周期表的第七周期
C.主要化合价为-4价.+4价
D.电解硝酸铜与硝酸“类铅”的混合溶液时首先会析出“类铅”
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某温度下,K(HCN)= 6.2×10-10 mol·L-1、K(HF)= 6.8×10-4 mol·L-1、K(CH3COOH)= 1.8×10-5 mol·L-1、、K(HNO2)= 6.4×10-6mol·L-1。物质的量浓度均为0.1 mol·L-1的下列溶液中,pH最小的是 ( )
A.NaCN B.NaF C.CH3COONa D.NaNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
物质氧化性、还原性的强弱,不仅与物质的性质有关,还与物质的浓度、温度、反应物用量等有关。下列各组物质中由于浓度、温度、用量等条件不同而能发生不同氧化还原反应的是
①Cu与HNO3溶液;②Fe与HCl溶液;③Zn与H2SO4溶液;
④铝与NaOH溶液; ⑤FeI2与Br2水; ⑥NH3与Cl2。
A.全部 B.①③④⑥ C.①②④⑤ D.①③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
近年来,酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。
(1)有人提出了一种利用氯碱工业产品处理含二氧化硫废气的方法,流程如下:
(Ⅰ)将含SO2的废气通入电解饱和食盐水后所得到的溶液中,得NaHSO3溶液。
(Ⅱ)将电解饱和食盐水所得气体反应后制得盐酸。
(Ⅲ)将盐酸加入NaHSO3溶液中,反应所得到的SO2气体回收,生成的NaCl循环利用。
①写出步骤(Ⅰ)反应的化学方程式:_________________________ _____________________________________________________。
②写出步骤(Ⅱ)中电解饱和食盐水的化学方程式:________________ ______________________________________________________________。
③写出步骤(Ⅲ)反应的离子方程式:_____________________________。
(2)还有学者提出利用Fe2+、Fe3+等离子的催化作用,常温下将SO2氧化成SO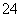 而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成SO
而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成SO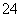 的转化率。
的转化率。

①该小组采用下图装置在实验室测定模拟烟气中SO2的体积分数,X溶液可以是________。(填写序号)
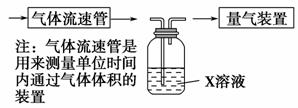
A.碘的淀粉溶液 B.酸性高锰酸钾溶液
C.氢氧化钠溶液 D.氯化钡溶液
②若上述实验是在标准状况下进行的,欲测定转化器中SO2氧化成SO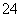 的转化率,已知气体流速,还需测定的数据有____________________________、_________________________。
的转化率,已知气体流速,还需测定的数据有____________________________、_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com