


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生活中钢铁制品生锈主要是由于吸氧腐蚀所致 |
| B、石油的裂化、裂解和煤的干馏都属于化学变化 |
| C、天然纤维、人造纤维、合成纤维组成元素相同 |
| D、工业废水中的Cu2+、Hg2+等重金属阳离子可以通过加入FeS除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:
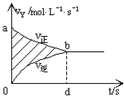 在容积固定的1L密闭容器里,进行可逆反应:X(g)+Y(g)?2Z(g),并达到平衡,在此过程中,以Y的浓度改变表示的反应速率v(正)、v(逆)与时间t的关系如图,结合题设条件,图中阴影部分面积不能表示( )
在容积固定的1L密闭容器里,进行可逆反应:X(g)+Y(g)?2Z(g),并达到平衡,在此过程中,以Y的浓度改变表示的反应速率v(正)、v(逆)与时间t的关系如图,结合题设条件,图中阴影部分面积不能表示( )| A、Z的浓度增加 |
| B、Y的物质的量减少 |
| C、X的浓度减少 |
| D、Y的浓度减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na、Mg、Al原子的最外层电子数依次减少 |
| B、C、N、O的原子半径依次减小 |
| C、Si、P、S元素的最高正化合价依次降低 |
| D、Li、Na、K的金属性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com