
分析 Ⅰ.该反应是正反应气体体积减小的放热反应,若提高氨合成反应速率,同时使平衡向氨合成方向移动,从影响化学反应速率的因素和影响平衡移动的因素综合考虑,只能是温度、浓度、压强三方面因素,所以可能是增大了反应物浓度,增大了压强,不可能是升温,因为升温平衡逆向移动,据此分析;
Ⅱ.(1)依据热化学方程式和盖斯定律计算得到所需热化学方程式得到反应焓变的关系;
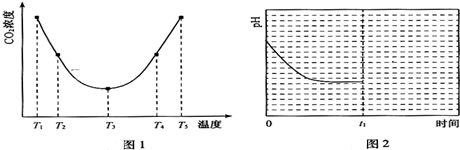
(2)①T1-T2区间,化学反应未达到平衡状态,温度越高,化学反应速率越快,所以CO2被捕获的量随着温度的升高而提高.T3-T4区间,化学反应已达到平衡状态,由于正反应为放热反应,温度升高平衡向逆反应方向移动,所以不利于CO2的捕获;
②反应Ⅲ在温度为T1时建立平衡后(由图2可知:溶液pH不随时间变化而变化),迅速上升到T2并维持温度不变,平衡逆向移动,溶液pH增大,在T2时又建立新的平衡.
解答 解:Ⅰ.N2(g)+3H2(g)?2NH3(g)△H<0,该反应是正反应气体体积减小的放热反应,若提高氨合成反应速率,同时使平衡向氨合成方向移动,从影响化学反应速率的因素和影响平衡移动的因素综合考虑,只能是温度、浓度、压强三方面因素的正增长,所以可能是增大了反应物浓度,增大了压强,不可能是升温,因为升温平衡逆向移动,降温、减压或减小生成物浓度时,反应速率减慢,
①升高温度增大反应速率,平衡逆向进行,故①错误;
②缩小容器体积(加压),压强增大,反应速率增大,平衡正向进行,有利于合成氨,故②正确;
③选择高效催化剂,改变反应速率,但不改变化学平衡,平衡不变,故③错误;
④在恒容条件下,再充入合成氨的原料气(N2、H2),相当于增大压强,反应速率增大,平衡正向进行,有利于合成氨,故④正确;
⑤在恒容条件下,再充入原平衡的混合气,相当于增大体系压强,反应速率增大,平衡正向进行,有利于合成氨,故⑤正确;
⑥在恒容条件下,分离出氨气,反应速率减小,平衡正向进行,不能增大反应速率,故⑥错误.
故答案为:②④⑤;
Ⅱ.(1)反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)?(NH4)2CO3(aq)△H1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)?(NH4)2HCO3(aq)△H2
反应Ⅲ:(NH4)2O3(aq)+H2O(l)+CO2(g)?2(NH4)2HCO3(aq)△H3
2×反应Ⅱ-反应Ⅰ得到反应Ⅲ的热化学方程式:(NH4)2O3(aq)+H2O(l)+CO2(g)?2(NH4)2HCO3(aq)△H3=2△H2-△H1,
故答案为:2△H2-△H1;
(2)①T1-T2区间,化学反应未达到平衡,温度越高,化学反应的速率越快,所以CO2被捕获的量随温度升高而提高,T4-T5区间,化学反应已达到平衡,由于正反应是放热反应,温度升高平衡向逆反应方向移动,所以不利于CO2的捕获,在T3前反应未建立平衡,无论在什么温度下(NH4)2CO3 (aq)总是捕获CO2,故c(CO2)减小,
故答案为:T1-T2区间,化学反应未达到平衡,温度越高,反应速率越快,所以CO2被捕获的量随温度的升而提高.T4-T5区间,化学反应已到达平衡,由于正反应是放热反应,温度升高,平衡向逆反应方向移动,所以不利于CO2的捕获;
②反应Ⅲ在温度为T1时建立平衡后(由图2可知:溶液pH不随时间变化而变化),迅速上升到T2并维持温度不变,平衡逆向移动,溶液pH增大,在T2时又建立新的平衡,图象应为,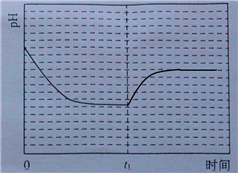 ,
,
故答案为: .
.
点评 本题考查了热化学方程式书写,化学反应速率、化学平衡移动和化学方程式书写等,影响化学反应速率和影响平衡移动的因素,注意知识的迁移和应用是关键,难度较大.


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 往硫化氢水溶液中加碱有利于S2-的增加 | |
| B. | 加入催化剂有利于氨氧化的反应 | |
| C. | 高压不利于合成氨的反应 | |
| D. | 500℃左右比室温更有利于合成氨的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.24 L | B. | 1.12 L | C. | 0.672 L | D. | 0.448 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4Q1+0.5Q2 | B. | 4Q1+Q2+10Q3 | C. | 4Q1+2Q2 | D. | 4Q1+0.5Q2+9Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入水时,溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 | |
| B. | 加入少量NaOH固体,平衡向逆反应方向移动,电离平衡常数减小 | |
| C. | 加入少量0.1 mol•L-1HCl溶液,溶液中c(OH-)增大 | |
| D. | 降低温度,溶液中c(NH4+)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,1 L 0.1 mol•L-1 NH4NO3溶液中NH4+、NO3-的数目均为0.1NA | |
| B. | 标准状况下,22.4 L N2和O2的混合气体中含有的原子总数为2NA | |
| C. | 常温常压下,16 g CH4中含有共价键的数目为NA | |
| D. | 16 g CH4与18 g NH4+所含质子数均为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 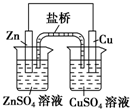 装置中,盐桥(含琼脂的饱和KCl溶液)中的K+移向ZnSO4溶液 | |
| B. | 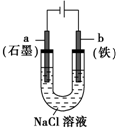 装置通电一段时间后溶液中有红褐色物质产生 | |
| C. | 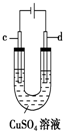 用装置精炼铜时,c极为粗铜 | |
| D. | 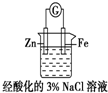 装置中电子由Zn电极沿外电路流向Fe电极,装置中有Fe2+生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(NH3)=0.010mol/(L.s) | B. | v(O2)=0.010mol/(L.s) | ||
| C. | v(NO)=0.0010mol/(L.s) | D. | v(H2O)=0.045mol/(L.s) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com