
| A. | 气态氢化物的稳定性:X<Z<W | |
| B. | X、Z、W氧化物对应水化物酸性的强弱顺序为Z<X<W | |
| C. | 室温下,含Y元素的盐形成的水溶液其pH<7 | |
| D. | Z元素的单质和氧化物均既能与NaOH溶液反应也能与某种酸反应 |
分析 Y元素的单质既能与盐酸反应也能与NaOH溶液反应,应为Al元素,Z原子的最外层电子数是次外层电子数的一半,应为Si元素,X与Z位于同一主族,则X为C元素,Y、Z、W原子的最外层电子数之和为14,则W的最外层电子数为14-3-4=7,且原子序数最大,应为Cl元素,结合元素周期律的递变规律判断元素对应的单质、化合物的性质.
解答 解:Y元素的单质既能与盐酸反应也能与NaOH溶液反应,应为Al元素,Z原子的最外层电子数是次外层电子数的一半,应为Si元素,X与Z位于同一主族,则X为C元素,Y、Z、W原子的最外层电子数之和为14,则W的最外层电子数为14-3-4=7,且原子序数最大,应为Cl元素,
A.气态氢化物的稳定性应该是:Z<X<W,故A错误;
B.只能判断X、Z、W最高价氧化物对应水化物酸性的强弱顺序为Z<X<W,故B错误;
C.Y是铝元素,含铝元素的盐如AlCl3水溶液显酸性,NaAlO2水溶液显碱性,故C错误;
D.硅和二氧化硅既能与NaOH溶液反应也能与氢氟酸反应,故D正确;
故选D.
点评 本题考查元素的推断及元素化合物的性质,题目难度中等,注意从物质的性质作为推断题的突破口,注意常见既能与盐酸反应也能与NaOH溶液反应的物质,题中从常见元素化合物的性质入手考查,是一道位置、结构、性质有机结合综合考查学生分析能力、推断能力的典型题目,难度较大.


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CHBrCH2Br | B. | CH3CH(CH2Br)2 | C. | CH3CHBrCHBrCH3 | D. | (CH3)2CBrCH2Br |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能量守恒原理 | B. | 泡利原理 | C. | 能量最低原理 | D. | 洪特规则 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
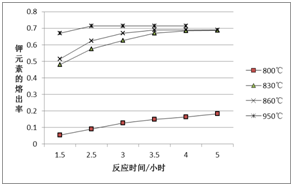 一定温度范围内用氯化钠熔浸钾长石(主要成份为KAlSi3O8)可制得氯化钾,主要反应是:NaCl(l)+KAlSi3O8(s)?KCl(l)+NaAlSi3O8(s)+Q.
一定温度范围内用氯化钠熔浸钾长石(主要成份为KAlSi3O8)可制得氯化钾,主要反应是:NaCl(l)+KAlSi3O8(s)?KCl(l)+NaAlSi3O8(s)+Q.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 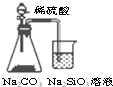 装置可比较硫、碳、硅三种元素的非金属性强弱 | |
| B. | 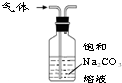 装置可除去CO2中少量的SO2杂质 | |
| C. | 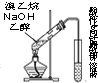 装置可用于检验溴乙烷与NaOH的醇溶液共热产生的乙烯 | |
| D. | 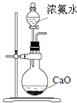 装置可用于实验室制备氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0 mol•L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl- | |
| C. | 与铝反应产生大量氢气的溶液:Na+、K+、CO32-、Cl- | |
| D. | pH=12的溶液:K+、Na+、CH3COO-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 土壤中离子的吸附和交换过程,有保肥作用 | |
| B. | 由肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 | |
| C. | 水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染 | |
| D. | 臭氧、Cl2均可用于水的消毒净化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作 | 现象 | 结论 |
| A | 向盐酸酸化的Ba(NO3)2溶液中通入SO2 | 有白色沉淀生成 | BaSO3难溶于酸 |
| B | 向等浓度的KCl、Kl混合液中滴加AgNO3溶液 | 先出现白色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 溴乙烷与NaOH水溶液共热后,加HNO3酸化,滴加AgNO3溶液 | 出现淡黄色沉淀 | 溴乙烷含溴元素 |
| D | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点:H2O>H2Se>H2S | B. | 酸性:H2SO4>H2CO3>HClO | ||
| C. | 硬度:I2>Br2>Cl2 | D. | 碱性:KOH>NaOH>Al(OH)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com