
| A. | A2B3是三氧化二铝 | B. | A3+与B2-最外层上的电子数相同 | ||
| C. | A是第2周期第ⅢA族的元素 | D. | B是第3周期第ⅥA族的元素 |
分析 由两种短周期元素A和M形成的离子化合物A2B3,A3+离子比B2-离子少一个电子层,则A和M都属于第三周期,且A3+具有与Ne原子相同的核外电子层结构,则A是Al元素,B是S元素,以此解答该题.
解答 解:由两种短周期元素A和M形成的离子化合物A2B3,A3+离子比B2-离子少一个电子层,则A和M都属于第三周期,且A3+具有与Ne原子相同的核外电子层结构,则A是Al元素,B是S元素,
A.根据以上分析知化合物A2B3是Al2S3,故A错误;
B.铝离子的结构示意图为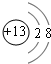 ,硫离子的结构示意图为
,硫离子的结构示意图为 ,则A3+与B2-最外层上的电子数相同,故B正确;
,则A3+与B2-最外层上的电子数相同,故B正确;
C.A是Al元素,Al元素位于第三周期第IIIA族,故C错误;
D.B是S元素,S元素位于第三周期第VIA族,故D错误;
故选B.
点评 本题考查了元素位置、结构、性质的相互关系及应用,正确推断元素是解本题关键,结合原子、离子的结构来分析解答,难度中等.


 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:多选题
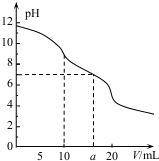 常温下,用 0.1mol•L HCl溶液滴定10.0mL浓度为0.1mol•L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,用 0.1mol•L HCl溶液滴定10.0mL浓度为0.1mol•L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )| A. | 当V=0时:c(H+)+c(H2CO3)+c(HCO3-)=c(OH-) | |
| B. | 当V=5时:c(Na+ )>c(HCO3-)>c(CO32- )>c(Cl- ) | |
| C. | 当V=a时:c(Na +)>c(Cl- )>c(H+ )=c(OH- ) | |
| D. | 当V=10时:c(H+ )+c(H2CO3)=c(OH- )+c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=3的HNO3与pH=11的KOH溶液 | |
| B. | pH=3的HNO3与pH=11的氨水 | |
| C. | pH=3的H2SO4与pH=11的NaOH | |
| D. | pH=3的CH3COOH 与pH=11的Ba(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
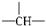 ,a个CH 3,其余为OH,则该物质分子中OH的个数可能为( )
,a个CH 3,其余为OH,则该物质分子中OH的个数可能为( )| A. | m-a | B. | n+m+a | C. | m+1-a | D. | m+2-a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
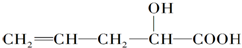 在不同条件下至少可能发生以下有机反应:①取代 ②加成 ③消去 ④氧化 ⑤酯化,其中跟其分子结构中-OH有关的可能反应为( )
在不同条件下至少可能发生以下有机反应:①取代 ②加成 ③消去 ④氧化 ⑤酯化,其中跟其分子结构中-OH有关的可能反应为( )| A. | ①②④⑤ | B. | ①②③⑤ | C. | ②③④⑤ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
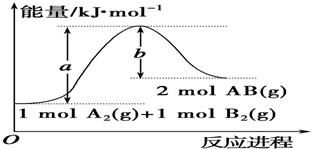
| A. | 每生成2分子AB吸收b kJ热量 | |
| B. | 该反应吸收热量 (a-b)kJ | |
| C. | 该反应中反应物的总能量低于生成物的总能量 | |
| D. | 断裂1mol A-A和1mol B-B键,放出a kJ能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
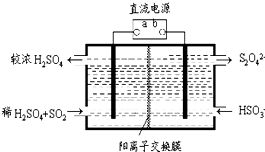 氮和硫的氧化物有多种,其中SO2和NOx都是大气污染物,对它们的研究有助于空气的净化.
氮和硫的氧化物有多种,其中SO2和NOx都是大气污染物,对它们的研究有助于空气的净化.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com