
【题目】食盐是日常生活的必需品,也是重要的化工原料。粗食盐常含有少量CaCl2、MgCl2、Na2SO4等杂质,实验室提供的试剂如下:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液。实验室提纯NaCl的流程如图:
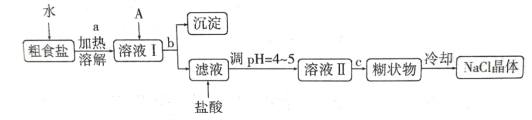
(1)欲除去溶液I中的杂质,写出A所代表的多种试剂,按滴加顺序依次为I.NaOH;Ⅱ.___________;Ⅲ.____________ (填化学式)。
(2)请写出下列试剂加入时发生反应的化学方程式:
①加入试剂I: ____________________________。
②加入盐酸:______________________________________________________.
(3)操作a、b中均用到的玻璃仪器是________、_______(填仪器名称),操作c的名称为___________________。
(4)如何对操作b所得到的沉淀进行洗涤:________________________。
(5)经过操作b后,如何检验所得溶液中的SO42-已除去:______________。
(6)若上述流程中未进行操作b,即直接向溶液I中加盐酸到pH为45,过滤,得到沉淀X和溶液Y,则沉淀X为__________(写化学式)。
【答案】BaCl2 Na2CO3 MgCl2+2NaOH=Mg(OH)2↓+2NaOH NaOH+HCl=NaCl+H2O Na2CO3+2HCl=2NaCl+H2O+CO2↑ 烧杯、玻璃棒 蒸发浓缩 在漏斗中加入蒸馏水没过沉淀,待洗涤液自然流干后,重复操作2~3次 取少许溶液于试管中,向其中加入BaCl2溶液,若无沉淀则证明SO42-已除去 BaSO4
【解析】
粗食盐常含有少量CaCl2、MgCl2、Na2SO4等杂质,由实验可知,加热溶解后,加NaOH除去Mg2+,加氯化钡除去SO42-,加碳酸钠除去Ca2+、Ba2+,碳酸钠一定在氯化钡之后,然后过滤,滤液中加盐酸除去过量氢氧化钠、碳酸钠溶液,调节pH后蒸发浓缩冷却后得到NaCl。
(1)欲除去溶液Ⅰ中的Ca2+、Mg2+、SO42-离子,应首先加入过量的氢氧化钠除去镁离子,然后加入过量的氯化钡可以除去硫酸根离子,最后加入过量的饱和碳酸钠溶液除去过量的钡离子和钙离子,故Ⅱ为BaCl2溶液;Ⅲ为饱和Na2CO3溶液;
(2)加入氢氧化钠后氢氧根离子与镁离子反应生成氢氧化镁沉淀,化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaOH;加入盐酸,可分别与滤液中的NaOH、碳酸钠反应,反应的化学方程式为:NaOH+HCl=NaCl+H2O、Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(3)操作a、b分别为溶解、过滤,都用到烧杯、玻璃棒,c为蒸发浓缩;
(4)对操作b所得到的沉淀进行洗涤:在漏斗中加入蒸馏水没过沉淀,待洗涤液自然流干后,重复操作2~3次;
(5)经过操作b后,检验所得溶液中的SO42-已除去:取少许溶液于试管中,向其中加入BaCl2溶液,若无沉淀则证明SO42-已除去;
(6)若上述流程中未进行操作b,加入盐酸后氢氧化镁、碳酸钡、碳酸钙溶解,硫酸钡不溶解,沉淀X为BaSO4。


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:
【题目】二环[1,0,0]丁烷(![]() )是最简单的桥环化合物。下列关于该化合物的说法错误的是
)是最简单的桥环化合物。下列关于该化合物的说法错误的是
A. 该化合物的二溴代物有4种
B. 生成1molC4H10需要2molH2
C. 该化合物与1,3-丁二烯互为同分异构体
D. 该化合物中4个碳原子可能处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室根据“侯氏制碱法”原理制备少量NaHCO3:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl。其实验包括制取氨气→ 制取NaHCO3→分离NaHCO3→干燥NaHCO3 四个步骤。下列实验必须选用的主要仪器正确的是:
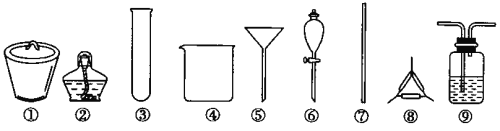
A. 制取氨气,可选用②③
B. 制取NaHCO3,可选用④⑦⑨
C. 分离NaHCO3,可选用④⑤⑥⑦
D. 干燥NaHCO3,可选用②③⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:
(1)配平下列化学方程式,并标明电子转移的方向与数目:
________Fe(OH)3+________NaOH+________NaClO→________Na2FeO4+________NaCl+________H2O,___________
(2)该反应中还原产物是________(填写化学式),________元素被氧化,氧化剂的电子式为________。
(3)当反应中有1mol Na2FeO4生成,转移的电子有________mol.
(4)如果配制250mL 0.1mol/L NaOH溶液,需要称取________g NaOH固体,所需的仪器有玻璃棒、胶头滴管、烧杯、________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,在我国部分海域中出现了大面积的“赤潮”,给当地渔业造成了重大损失,赤潮直接威胁着人类生存的环境,已经成为我国目前最主要的海洋灾害之一。下列关于赤潮发生原因的叙述正确的是
A. 含氯化合物直接排入大海,引起赤潮的发生。
B. 赤潮发生的根本原因是含氟制冷剂大量使用导致臭氧层破坏的结果。
C. 含氮、磷的大量污水直接排入大海,导致某些浮游生物爆发性繁殖是赤潮发生的直接原因。
D. 空气中二氧化碳浓度升高,导致海洋温度升高,引起了赤潮的发生。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物——光化学烟雾,其中某些反应过程如图所示。下列说法不正确的是
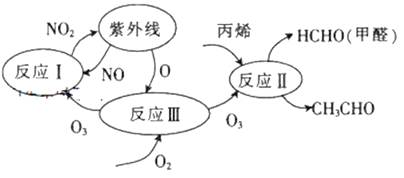
A. 整个过程中O3作催化剂
B. 反应III的方程式为O2+O===O3
C. 光化学烟雾中含甲醛、乙醛等刺激性物质
D. 反应I、反应Ⅱ均属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符合的是

A. 图甲表示对某化学平衡体系改变温度后反应速率随时间的变化
B. 图乙表示反应物断键吸收的能量大于生成物成键放出的能量
C. 图丙表示0.1 mol·L-1NaOH溶液滴定20 mL 0.1 mol·L-1硫酸时溶液pH的变化
D. 图丁表示向Ba(OH)2溶液中滴加稀H2SO4至过量,溶液的导电性变化情况
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) A元素的原子最外层电子数是次外层电子数的2倍,则该元素的原子核内质子数____。
(2)已知铁(Fe)原子的核内质子数为26,核外共有4个电子层,最外电子层上的电子数是2,写出铁原子的结构示意图:_____。
(3) a元素原子M电子层上有6个电子,b元素与a元素的原子核外电子层数相同,b元素的原子最外层电子数为1。a、b两种元素形成的化合物名称是______。该化合物在无色火焰上燃烧时,火焰呈____色。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值。下列说法正确的是
A. 常温常压下,11.2L甲烷中含有的共价键数为2NA
B. 1 mol OH-中含有9NA个电子
C. 1L1mol·L-1AlCl3溶液中含有NA个Al3+
D. 3.2g由O2和O3组成的混合气体中含有的氧原子数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com