
以BaS为原料制备Ba(OH)2·8H2O的过程是:BaS与HCl反应,所得溶液在70~90℃时与过量NaOH溶液作用,除杂,冷却后得到Ba(OH)2·8H2O晶体.据最新报道,生产效率高、成本低的Ba(OH)2·8H2O晶体的新方法是使BaS与CuO反应……
(1)新方法的反应方程式为________.
(2)该反应反应物CuO是不溶物,为什么该反应还能进行:________.
(3)简述新方法生产效率高、成本低的原因.
|
答案:(1)BaS+CuO+9H2O=Ba(OH)2·8H2O+CuS(也可写Ba(OH)2.); (2)CuS的溶度积比CuO小得多(更难溶),有利于该反应正向进行; (3)CuS为难溶物(未反应的CuO也不溶),过滤后,将滤液浓缩、冷却,就可在溶液中析出Ba(OH)2·8H2O晶体,故生产效率高;CuS在空气中焙烧氧化可得CuO与SO2,故CuO可反复使用(SO2可用于制硫的化合物),因而成本低. 思路与技巧:本题的方程式通过审题可知,反应物为BaS与CuO,生成物之一为Ba(OH)2·8H2O,根据元素守恒,反应物中必有水,生成物中必有CuS沉淀.该反应之所以进行,根据沉淀转化可知必然是生成溶解度更小的物质.生产效率、生产成本的问题关键是通过审题从题目中找出要素结合反应原理进行分析.该类问题要留意,这是新课改的亮点. |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解

| ||
| ||
| 高温 |
查看答案和解析>>
科目:高中化学 来源:2014届四川省邛崃市高三第一次月考理综化学试卷(解析版) 题型:填空题
Ⅰ.将由Na+、Ba2+、Cu2+、SO42-、Cl-组合形成的三种强电解质溶液,分别装入下图装置中的甲、乙、丙三个烧杯中进行电解,电极均为石墨电极。
接通电源,经过一段时间后,测得乙中c电极质量增加。常温下各烧杯中溶液pH与电解时间t的关系如右上图(忽略因气体溶解带来的影响)。据此回答下列问题:

(1)在甲中烧杯中滴加酚酞, 极(填a或b)附近溶液会变红。
(2)写出乙烧杯中发生反应的化学方程式 。
(3)电极f上发生的电极反应式为 。
(4)若经过一段时间后,测得乙烧杯中c电极质量增加了8g,要使丙烧杯中溶液恢复到原来的状态,应进行的操作是 。
Ⅱ.工业上利用BaSO4制备BaCl2的工艺流程如下:
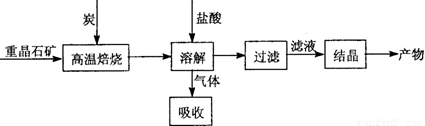
某活动小组的同学在实验室以重晶石(主要成分BaSO4)为原料,对上述工艺流程进行模拟实验。
(1)上述过程中,气体用过量NaOH溶液吸收得到Na2S。Na2S水溶液显碱性的原因是 。(用离子方程式表示)
(2)已知有关反应的热化学方程式如下:
BaSO4(s) +4C(s) 4CO(g)+BaS(s)
△H1 =
+571.2kJ/mol ①
4CO(g)+BaS(s)
△H1 =
+571.2kJ/mol ①
C(s) +CO2(g) 2CO(g)
△H2 =
+172.5kJ/mol
②
2CO(g)
△H2 =
+172.5kJ/mol
②
则反应BaSO4(s)
+2C(s) 2CO2(g)
+ BaS(s) △H3 =
2CO2(g)
+ BaS(s) △H3 =
(3)在高温焙烧重晶石过程中必须加入过量的炭,同时还要通入空气,其目的是 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年北京市昌平区高三上学期期末考试理综化学试卷(解析版) 题型:填空题
硫酸盐在生产生活中有广泛应用。
Ⅰ.工业上以重晶石(主要成分BaSO4)为原料制备BaCl2,其工艺流程示意图如下:
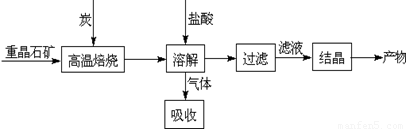
某研究小组查阅资料得:
BaSO4(s)+4C(s) 4CO(g)+BaS(s)△H1=+571.2kJ•mol-1
①
4CO(g)+BaS(s)△H1=+571.2kJ•mol-1
①
BaSO4(s)+2C(s) 2CO2(g)+BaS(s)△H2=+226.2kJ•mol-1
②
2CO2(g)+BaS(s)△H2=+226.2kJ•mol-1
②
(1)用过量NaOH溶液吸收气体,得到硫化钠。该反应的离子方程式是 。
(2)反应C(s)+CO2(g) 2CO(g)的△H= 。
2CO(g)的△H= 。
(3)实际生产中必须加入过量的炭,同时还要通入空气,其目的有两个
①从原料角度看, ;
②从能量角度看,①②为吸热反应,炭和氧气反应放热维持反应所需高温。
(4)该小组同学想对BaSO4在水中的沉淀溶解平衡做进一步研究,查资料发现在某温度时BaSO4在水中的沉淀溶解平衡曲线如图所示。
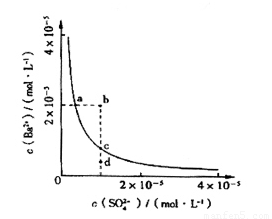
该小组同学提出以下四种观点:
①当向含有SO42-的溶液中加入Ba2+ 使SO42-沉淀完全,则此时SO42-在溶液中的浓度为0
②加入Na2SO4可以使溶液由a点变到b点
③通过蒸发可以使溶液由d点变到c点
④d点无BaSO4沉淀生成
其中正确的是 (填序号)。
Ⅱ.某燃料电池以CaHSO4固体为电解质传递H+,其基本结构如图所示,电池总反应可表示为2H2+O2═2H2O。
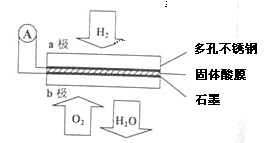
请回答:
(5)H+由 极通过固体酸电解质传递到另一极(填a或者b)。
(6)b极上发生的电极反应是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com