
| A. | 该溶液中,H+、NH4+、SO42-、Br-可以大量共存 | |
| B. | 该溶液中,Ag+、K+、NO3-、CH3CHO可以大量共存 | |
| C. | 向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+═Cl-+2Fe3++H20 | |
| D. | 向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个 |
分析 A、次氯酸为弱酸,次氯酸根与氢离子不能大量共存;
B、银离子与氯离子生成AgCl白色难溶沉淀,故而不能电离共存;
C、NaClO为强碱弱酸盐,水解呈碱性,NaCl为中性,溶液中不存在大量的氢离子;
D、次氯酸具有氧化性,浓盐酸具有还原性,两者发生归中反应生成氯气,据此解答即可.
解答 解:A、NaClO和NaCl混合溶液中存在大量的次氯酸根,次氯酸为弱酸,次氯酸根与氢离子不能大量共存,故A错误;
B、NaClO和NaCl混合溶液中存在大量的氯离子,与银离子反应生成白色难溶沉淀,故不能大量共存,故B错误;
C、NaClO为强碱弱酸盐,水解呈碱性,NaCl为中性,溶液中不存在大量的氢离子,与2Fe2++ClO-+2H+═Cl-+2Fe3++H20反应矛盾,故C错误;
D、浓盐酸中Cl由-1价升高到0价,次氯酸中Cl由+1价降低到0价,故每生成1mol氯气转移电子数为1mol,故D正确,故选D.
点评 本题主要考查的是溶液中离子的判断,涉及离子共存、盐类水解、氧化还原反应原理等,综合性较强,容易出错的是C选项,没有注意原溶液的酸碱性.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 1.7 | B. | 2.0 | C. | 12.0 | D. | 12.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1 的硫酸溶液中NH4+、Fe2+、Cl-、NO3-可以共存 | |
| B. | 向Ba(OH)2 溶液中滴入硫酸溶液的离子方程式为:Ba2++SO42-═BaSO4↓ | |
| C. | 0.1mol•L-1 AlCl3 溶液,温度从20℃升高到50℃,所有离子浓度均增大 | |
| D. | pH=11的NaOH 溶液中有:[OH-]=[Na+]+[H+] |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
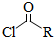 )偶联可用于制备药物Ⅱ:
)偶联可用于制备药物Ⅱ: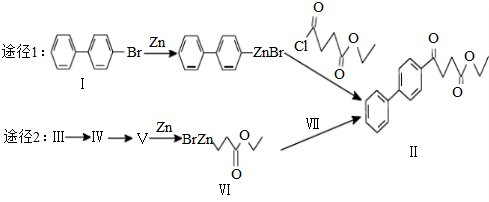
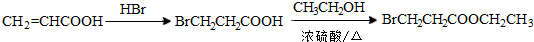 .(标明反应试剂,忽略反应条件).
.(标明反应试剂,忽略反应条件).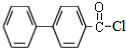 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 结论 |
| 实验1:在盛有不含O2的25mL0.1mol•L-1BaCl2溶液的烧杯中,缓慢通入纯净的SO2气体. | 无现象 | 假设一成立 |
| 实验2:在盛有不含O2的25mL0.1mol•L-1Ba(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体 | 生成白色沉淀 |

| 实验步骤、预期现象和结论(不要求写具体操作过程): |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
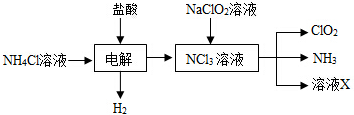

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
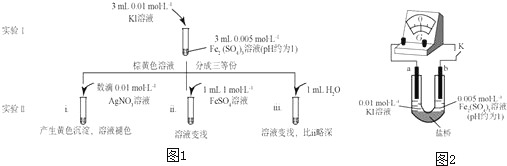
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 合金贮氢材料具有优异的吸放氢性能,在配合氢能的开发中起到重要作用.
合金贮氢材料具有优异的吸放氢性能,在配合氢能的开发中起到重要作用.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com