
实验室制取氯气如下图,连接好实验装置.

(1)连接好装置后,先________.
(2)向烧瓶里加入少量________粉末,分液漏斗中注入密度为1.19 g·cm-3的________,慢慢地将分液漏斗中的液体注入烧瓶.
(3)用________加热,氯气便能放出.
(4)A中盛放的是________,其作用为________.
(5)B中盛放的是________,其作用为________.
(6)C的要求和作用是________.
(7)D中盛放的是________,其作用为________.
(8)从中可以得出氯气的物理性质为________.
科目:高中化学 来源: 题型:

(1)连接好装置后,先___________。
(2)向烧瓶里加入少量___________粉末,分液漏斗中注入密度为1.19 g·cm-3的___________,慢慢地将分液漏斗中的液体注入烧瓶。
(3)___________加热,氯气便能放出。
(4)A中盛放的是___________,其作用为__________________________________。
(5)B中盛放的是___________,其作用为__________________________________。
(6)C的要求和作用是_______________________________________________。
(7)D中盛放的是___________,其作用为_________________________________。
(8)从中可以得出氯气的物理性质为__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:


完成下列问题:
(1)写出实验中制备氯气的化学反应方程式:________________________________。
(2)对于乙同学的实验装置,要停止实验应怎样操作________________________。
(3)甲、乙两同学分别向收集到的氯气中加入适量的水,充分振荡后分成两份,均做验证氯气与水反应所得产物性质的两个实验。实验操作、现象、结论均相同。
记录如下:
实验序号 | 实验操作 | 现象 | 结论 |
① | 加品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
② | 加入NaHCO3粉末 | 有无色气泡产生 | 氯气与水反应的产物有较强的酸性 |
请你评价甲、乙两同学得出实验①②的结论是否合理?若不合理,请说明理由____________
_____________________________。
(4)丙同学查阅资料发现,HClO的氧化性大于MnO2,拟用下列四组试剂在实验室制取氯气:
A.CaCl2和次氯酸 B.浓盐酸和NaClO
C.浓盐酸和次氯酸 D.固体NaCl、固体NaClO和浓硫酸
你认为上述四组试剂中____________组试剂既符合实际,且Cl的利用率最高,写出这个反应的化学方程式:________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学实验兴趣小组进行实验室制取氯气,并验证氯气的某些化学性质实验,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
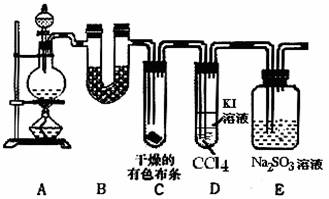
(1)下列方法中,可制得氯气的正确组合是 。
① MnO2和浓盐酸混合共热; ② NaCl固体和浓硫酸混合共热;
③ 次氯酸钠和稀盐酸混合; ④ K2Cr2O7和浓盐酸混合;
⑤ KClO3和浓盐酸混合; ⑥ KMnO4和浓盐酸混合。
A.①②⑥ B.②④⑥ C.①③⑥ D.①④⑤⑥
(2)制取氯气时在烧瓶中加入一定量的MnO2,通过 (填仪器名称)
向烧瓶中加入适量的浓盐酸,该反应的离子方程式:
实验时为了除去氯气中的氯化氢气体,最好在A、B之间安装盛有 试剂的净化装置。
(3)①装置B中盛有 试剂(填序号)a.浓硫酸 b.碱石灰 c.五氧化二磷d无水氯化钙,其作用是
②装置C中的现象是
D中下层溶液的现象是
③装置E中发生反应的离子方程式为
(4)乙同学认为甲同学的实验有缺陷,提出在 位置后(填字母)增加一个装置,该装置中应放入 试剂,其作用是
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学实验兴趣小组进行实验室制取氯气,并验证氯气的某些化学性质实验,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题。

(1)下列方法中,可制得氯气的正确组合是 。
① MnO2和浓盐酸混合共热;② NaCl固体和浓硫酸混合共热;
③ 次氯酸钠和稀盐酸混合; ④ K2Cr2O7和浓盐酸混合;
⑤ KClO3和浓盐酸混合; ⑥ KMnO4和浓盐酸混合。
A.①②⑥ B.②④⑥ C.①③⑥ D.①④⑤⑥
(2)制取氯气时在烧瓶中加入一定量的MnO2,通过 (填仪器名称)向烧瓶中加入适量的浓盐酸,该反应的离子方程式: ;实验时为了除去氯气中的氯化氢气体,最好在A、B之间安装盛有 试剂的净化装置。
(3) 若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得Cl2的体积(标准状况下)
总是小于1.12 L的原因是
(4)①装置B中盛有 试剂(填序号)a.浓硫酸 b.碱石灰 c.五氧化二磷 d.无水氯化钙。其作用是
②装置C中的现象是 ;D中下层液体的现象是
③装置E中发生反应的离子方程式为
(5)乙同学认为甲同学的实验有缺陷,提出在 位置后(填字母)增加一个装置,该装置中应放入 试剂,其作用是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com