
某化学研究性学习小组对铜及铜的部分化合物的性质进行实验探究,研究的问题和过程如下:
I.氯化铜的制备
该研究性小组在实验室里用下列仪器和药品来制取纯净的无水氯化铜:
序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
仪器及装置图 |
|
|
|
|
|
|
图中A、B、C、D、E、F的虚线部分表示玻璃管接口,接口的弯曲和伸长等部分未画出。根据要求填写下列各小题空白:
(1)如果所制气体从左向右流动时,上述各仪器装置的正确连接顺序是(填各装置的序号)_____接_____接_____接_____接_____接;
(2)装置④的作用是_____________________;
(3)在装置⑤的烧瓶中,发生反应的化学方程式为_____________________;
Ⅱ.探究Cu(OH)2是否和Al(OH)3一样具有两性
(4)该研究性学习小组取适量实验I中制得的产品氯化铜固体充分溶解在一定浓度的盐酸中,过滤,得氯化铜溶液;为探究Cu(OH)2是否和Al(OH)3一样具有两性,除选择配制的CuCl2溶液外,还需要一定选用的试剂为________________;(填序号)
a.氨水 b.氢氧化钠溶液 c.稀硫酸 d.冰醋酸
Ⅲ.为探究不同价态铜的稳定性
(5)该研究性学习小组用实验Ⅱ中所获得的氢氧化铜沉淀制得氧化铜粉末,然后将CuO粉末加热至1000℃以上完全分解成红色的Cu2O粉末,该实验说明:在高温条件下,+l价的Cu比+2价Cu更________(填“稳定”或“不稳定”).
(6)向Cu2O中加适量稀硫酸,得到蓝色溶液和一种红色固体,该反应的离子化学方程式为___________;
科目:高中化学 来源:2015-2016学年西藏日喀则一中高二月考化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.稀硫酸和氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓
B.碳酸钠溶液与盐酸反应:Na2CO3+2H+=2Na++CO2↑+H2O
C.铁钉放入硫酸铁溶液中:Fe+Fe3+=2Fe2+
D.Ca(NO3)2溶液和Na2CO3溶液混合:Ca2++CO32-=CaCO3↓
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高二下期末化学试卷(解析版) 题型:选择题
下列物质中含有共价键的离子化合物是
A.Ba(OH)2 B.CaCl2 C.H2O D.H2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二下期末化学试卷(解析版) 题型:选择题
下列事实不能用键能的大小来解释的是
A. N元素的电负性较大,但N2的化学性质很稳定
B. 惰性气体一般难发生反应
C. HF、HCl、HBr、HI的稳定性逐渐减弱
D. F2比O2更容易与H2反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二下期末化学试卷(解析版) 题型:选择题
下列电子排布中,原子处于激发状态的是
A. 1s22s22p5
B. 1s22s22p43s2
C. 1s22s22p63s23p63d54s1
D. 1s22s22p63s23p63d34s2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南株洲二中等六校高二下期末化学试卷(解析版) 题型:选择题
现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(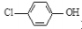 ),其原理如下图所示,下列说法正确的是
),其原理如下图所示,下列说法正确的是
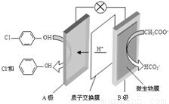
A.当外电路中有0.2mole-转移时,通过质子交换膜的H+的个数为0.2NA
B.A极的电极反应式为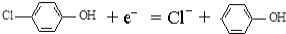
C.电流方向从B极沿导线经小灯泡流向A极
D.B极为电池的正极,发生还原反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南株洲二中等六校高二下期末化学试卷(解析版) 题型:选择题
设NA为阿伏加罗常数的数值,下列说法正确的是
A.一定条件下,2molSO2和1molO2混合在密闭容器中充分反应后容器中的分子数大于2NA
B.5.6g铁粉与足量水蒸汽反应生成的H2分子数目为0.1NA
C.向0.1mol/L的FeBr2溶液中通适量Cl2,当c(Br-)=0.1mol/L时,消耗Cl2的分子数为0.1NA
D.在反应Cu2S+O2 2Cu+SO2中,每生成1molCu,转移电子数目为2NA
2Cu+SO2中,每生成1molCu,转移电子数目为2NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二下期末模拟化学试卷(解析版) 题型:选择题
为探究外界条件对反应:mA(g)+nB(g) cZ(g) △H的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是
cZ(g) △H的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是
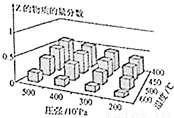
A.在恒温恒容条件下,向已达到平衡的体系中加入少量Z,平衡正向移动,Z的含量增大
B.升高温度,正、逆反应速率都增大,平衡常数增大
C.△H<0 m+n>c
D.△H>0 m+n<c
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西西北大学附中高二下期末化学试卷(解析版) 题型:填空题
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。

(1)T、X、Y原子的第一电离能由小到大的顺序是____________(用元素符号表示)。
(2)LX2分子的电子式是________________,XY2分子是____________(填“极性分子”或“非极性分子”);QY3分子中Q采用________杂化。
(3)由J、L、R三种元素形成的某种配位化合物,该化合物具有挥发性,化学式J(LR)4,其中J的化合价是0价。则基态J原子的核外电子排布式是___________________________;写出与配位体微粒互为等电子体的离子、分子各一种________、________。
(4)由Z、L、Q三种元素组成的化合物,分子式为Z9L3Q,它有_________种同分异构体(其中Q以三个单键与其他原子相连),请写出其中沸点最低的物质的结构简式__________________。
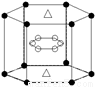
(5)A与M组成的一种化合物AM2,刷新了金属化合物超导温度的最高纪录。右图所示的是该化合物的晶体结构单元。图中上下底面中心“△”处的原子是________(填元素符号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com